|
 |
- Search
| Korean J Neuromuscul Disord > Volume 15(1); 2023 > Article |
|
ABSTRACT
Respiratory muscle weakness caused by neuromuscular disease can lead to both acute and chronic respiratory failure. Respiratory failure caused by Guillain-Barr├® syndrome and myasthenia gravis can potentially improve with disease-specific therapy. However, respiratory failure in amyotrophic lateral sclerosis is irreversible, and it may be necessary to provide full-time ventilation support along with additional assistance. Noninvasive ventilation is recommended for managing acute or acute-on-chronic hypercapnic respiratory failure caused by neuromuscular disease. It has also been effective in weaning patients off invasive mechanical ventilation. Although noninvasive ventilation offers numerous benefits over invasive mechanical ventilation, it is crucial to consider the specific contraindications and limitations of noninvasive ventilation and ensure its appropriate usage based on the patient's condition and needs. The timely recognition of neuromuscular respiratory failure is critical, as early intervention can be life-saving. This review focused on the clinical assessment and management of acute respiratory failure in neuromuscular diseases.
ĒśĖĒØĪĻ│äļŖö Ļ░ĆņŖżĻĄÉĒÖśņØ┤ ņØ╝ņ¢┤ļéśļŖö ĒÅÉņÖĆ ĒÅÉļź╝ ĒÖśĻĖ░ņŗ£ĒéżļŖö ĒÄīĒöäļĪ£ ĻĄ¼ņä▒ļÉ£ļŗż. ĒÄīĒöäļŖö ĒśĖĒØĪĻĘ╝ņØä ĒżĒĢ©ĒĢ£ ĒØēļ▓Į, ņżæņČöņŗĀĻ▓ĮĻ│äņØś ĒśĖĒØĪņĪ░ņĀłĻĖ░, ņżæņČö ĒśĖĒØĪņĪ░ņĀłĻĖ░ņÖĆ ĒśĖĒØĪĻĘ╝ņØä ņŚ░Ļ▓░ĒĢśļŖö ņ▓ÖņłśņÖĆ ļ¦Éņ┤łņŗĀĻ▓Įņ£╝ļĪ£ ĻĄ¼ņä▒ļÉ£ļŗż. ĒśĖĒØĪļČĆņĀäņØĆ ĒśĖĒØĪĻ│╝ņĀĢņŚÉņä£ ņĪ░ņ¦üņ£╝ļĪ£ ņé░ņåī ņĀäļŗ¼ņØ┤ ņל ļÉśņ¦Ć ņĢŖĻ▒░ļéś, ņĪ░ņ¦üņŚÉņä£ ņØ┤ņé░ĒÖöĒāäņåī ņĀ£Ļ▒░Ļ░Ć ņל ļÉśņ¦Ć ņĢŖļŖö ņāüĒā£ņØ┤ļŗż. ĒÅÉļĀ┤, ĒÅÉļČĆņóģ, ĒÅÉņāēņĀäņ”Ø ļō▒ ĒÅÉņ¦łĒÖśņ£╝ļĪ£ ņØĖĒĢ£ ĒśĖĒØĪļČĆņĀäņØĆ ņĀĆņé░ņåīĒśłņ”Ø(hypoxemia)ņØä ņ£Āļ░£ĒĢśĻ│Ā, ņĀĆņé░ņåīĒśłņ”ØĒśĖĒØĪļČĆņĀä ļśÉļŖö 1ĒśĢĒśĖĒØĪļČĆņĀäņØ┤ļØ╝Ļ│Ā ĒĢśĻ│Ā, ļ¦īņä▒ĒÅÉņćäĒÅÉņ¦łĒÖś, ņ▓£ņŗØ, ņĢĮļ¼╝, ļćīļ│æļ│ĆņØ┤ļéś ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ļō▒ņŚÉ ņØśĒĢ£ ĒśĖĒØĪļČĆņĀäņØĆ ĒÅÉĒżņĀĆĒÖśĻĖ░(alveolar hypoventilation)ņŚÉ ņØśĒĢ£ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”Ø(hypercapnia)ņØä ņ£Āļ░£ĒĢśĻ│Ā, Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØĒśĖĒØĪļČĆņĀä ļśÉļŖö 2ĒśĢĒśĖĒØĪļČĆņĀäņØ┤ļØ╝Ļ│Ā ĒĢ£ļŗż. ĒÅÉĒżņĀĆĒÖśĻĖ░ļŖö ņĀĆņé░ņåīĒśłņ”ØļÅä ņ£Āļ░£ĒĢśņ¦Ćļ¦ī Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ ĒŖ╣ņ¦ĢņĀüņØĖ ņåīĻ▓¼ņØ┤ļŗż[1]. ņØ┤ ņÖĖņŚÉ ļ¼┤ĻĖ░ĒÅÉņŚÉ ņØśĒĢ£ ĒśĖĒØĪļČĆņĀäņØä 3ĒśĢĒśĖĒØĪļČĆņĀä, ņć╝Ēü¼ņŚÉ ņØśĒĢ┤ ĒśĖĒØĪĻĘ╝ņ£╝ļĪ£ Ļ░ĆļŖö ĒśłņĢĪļ¤ēņØ┤ Ļ░ÉņåīĒĢśņŚ¼ ļ░£ņāØĒĢśļŖö ĒśĖĒØĪļČĆņĀäņØä 4ĒśĢĒśĖĒØĪļČĆņĀäņØ┤ļØ╝Ļ│Ā ĒĢ£ļŗż. ļ¼╝ļĪĀ ĒĢ£ ĒÖśņ×ÉņŚÉņä£ ņŚ¼ļ¤¼ ĒśĖĒØĪļČĆņĀäņØ┤ ļÅÖņŗ£ņŚÉ ņØ╝ņ¢┤ļéĀ ņłś ņ׳ļŗż[2]. ĒśĖĒØĪļČĆņĀäņØä ņ¦äļŗ©ĒĢśļŖö ņĀłļīĆņĀüņØĖ ĻĖ░ņżĆņØĆ ņŚåņ¦Ćļ¦ī, ņØ╝ļ░śņĀüņ£╝ļĪ£ 60 mmHg ļ»Ėļ¦īņØś ļÅÖļ¦źĒśłņé░ņåīļČäņĢĢ(PaO2), 45 mmHg ņØ┤ņāüņØś ļÅÖļ¦źĒśłņØ┤ņé░ĒÖöĒāäņåīļČäņĢĢ(PaCO2)ņØä ĻĖ░ņżĆņ£╝ļĪ£ ĒÅēĻ░ĆĒĢ£ļŗż[1]. ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņØś ņ╣śļŻīĻ░Ć ņ¦ĆņŚ░ļÉĀ Ļ▓ĮņÜ░ ĒśĖĒØĪņé░ņ”ØĻ│╝ ņŗ¼ĒÅÉņĀĢņ¦ĆĻ░Ć ņØ╝ņ¢┤ļéĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņĪ░ĻĖ░ņ¦äļŗ©Ļ│╝ ņ╣śļŻīĻ░Ć ĒĢäņÜöĒĢśļŗż[3].
ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉļŖö ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ņ×Éņ▓┤(ņśł: ĻĖ░ņ¢Ł-ļ░öļĀłņ”ØĒøäĻĄ░[Guillain-Barr├® syndrome, GBS] ņØ┤ļéś ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Ø), ĒśĖĒØĪĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢ┤ņä£ ļ░£ņāØĒĢśļŖö ĒĢ®ļ│æņ”Ø(ņśł: ĒØĪņØĖĒÅÉļĀ┤ņØ┤ļéś ļ¼┤ĻĖ░ĒÅÉ), ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśĻ│╝ ļÅÖļ░śļÉ£ ņŗ¼ĒÅÉņ¦łĒÖś(ņśł: ĻĖēņä▒ņÜĖĒśłņŗ¼ļČĆņĀäņØ┤ļéś ĒÅÉņāēņĀäņ”Ø)ņŚÉ ņØĖĒĢ┤ ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż. ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņØä ņ£Āļ░£ĒĢśļŖö Ļ░Ćņן ĒØöĒĢ£ ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņØĆ ĻĖ░ņ¢Ł-ļ░öļĀłņ”ØĒøäĻĄ░Ļ│╝ ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”ØņØ┤Ļ│Ā, ĻĘ╝ņ£äņČĢņĖĪņéŁĻ▓ĮĒÖöņ”ØņØ┤ļéś ņäĀņ▓£ĻĘ╝ņ£Īļ│æņ”Ø ĒÖśņ×ÉļŖö ļ¦īņä▒ĒśĖĒØĪļČĆņĀäņØ┤ ĒÅÉņØś ĒĢ®ļ│æņ”ØņØ┤ļéś ļÅÖļ░śļÉ£ ņŗ¼ĒÅÉņ¦łĒÖśņŚÉ ņØśĒĢ┤ ņĢģĒÖöļÉśņ¢┤ ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņ£╝ļĪ£ ņ¦äĒ¢ēĒĢĀ ņłś ņ׳ļŗż[4].
ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņŚÉņä£ ļéśĒāĆļéśļŖö ĒśĖĒØĪļČĆņĀäņØś ĻĖ░ņĀä, ņ¦äļŗ©, ņ╣śļŻī ļ░Å ĻĖ░ņ¢Ł-ļ░öļĀłņ”ØĒøäĻĄ░, ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Ø, ĻĘ╝ņ£äņČĢņĖĪņéŁĻ▓ĮĒÖöņ”ØņŚÉņä£ ļéśĒāĆļéśļŖö ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņŚÉ ļīĆĒĢ┤ ņé┤ĒÄ┤ļ│┤Ļ▓Āļŗż.
ĒśĖĒØĪĻĘ╝ņ£ĪņØĆ ļōżņł©ĻĘ╝ņ£Ī(inspiratory muscles), ļéĀņł©ĻĘ╝ņ£Ī(expiratory muscles), ņāüĻĖ░ļÅäĻĘ╝ņ£Ī(upper airway muscles)ņ£╝ļĪ£ ļéśļłī ņłś ņ׳ļŗż. ļōżņł©ĻĘ╝ņ£ĪņØĆ ĒÖśĻĖ░(ventilation)ļź╝ ļŗ┤ļŗ╣ĒĢśĻ│Ā, ļéĀņł©ĻĘ╝ņ£ĪņØĆ ĻĖ░ņ╣©ņØä ļŗ┤ļŗ╣ĒĢśļ®░, ņāüĻĖ░ļÅäĻĘ╝ņ£ĪņØĆ ĻĖ░ļÅäļź╝ ļ│┤ĒśĖĒĢśļŖö ņŚŁĒĢĀņØä ĒĢ£ļŗż.
ĒÜĪĻ▓®ļ¦ēņØĆ ņŻ╝ļÉ£ ļōżņł©ĻĘ╝ņ£Īņ£╝ļĪ£ Ē£┤ņŗØņāüĒā£ņŚÉņä£ ņØ╝ņ¢┤ļéśļŖö ļōżņł©ņØś 2/3 ņØ┤ņāüņØä ļŗ┤ļŗ╣ĒĢ£ļŗż. ļŹö ļ¦ÄņØĆ ĒÖśĻĖ░Ļ░Ć ĒĢäņÜöĒĢĀ ļĢīļŖö ļ░öĻ╣źĻ░łļ╣äņé¼ņØ┤ĻĘ╝(external intercostals), ļ¬®Ļ░łļ╣äĻĘ╝(scalenes), ļ¬®ļ╣ŚĻĘ╝(sternocleidomastoids) ļō▒ņØś ļŹöļČĆļōżņł©ĻĘ╝ņ£Ī(accessory inspiratory muscles)ņØ┤ ļōżņł©ņŚÉ Ļ┤ĆņŚ¼ĒĢ£ļŗż. ņĢłņĀĢņāüĒā£ņØś ļéĀņł©ņØĆ ņŻ╝ļĪ£ ĒÅÉņÖĆ ĒØēĻ│ĮņØ┤ ļōżņł©ņŚÉ ņØśĒĢ┤ ņŗĀņןļÉ£ ĒøäņŚÉ ņØ┤ļŻ©ņ¢┤ņ¦ĆļŖö ļ░śļÅÖ(recoil)ņŚÉ ņØśĒĢ┤ ņØ╝ņ¢┤ļéśĻ│Ā, Ļ░ĢĒĢ£ ļéĀņł©ņØ┤ ĒĢäņÜöĒĢĀ ļĢīļŖö ņåŹĻ░łļ╣äņé¼ņØ┤ĻĘ╝(internal intercostals)Ļ│╝ ļ░░ĻĘ╝ņ£ĪņØ┤ ļéĀņł©ņØä ļŗ┤ļŗ╣ĒĢ£ļŗż. ļ░░ĻĘ╝ņ£ĪņŚÉļŖö ļ░░ņåŹļ╣ŚĻĘ╝(internal oblique), ļ░░ļ░öĻ╣źļ╣ŚĻĘ╝(external oblique), ļ░░Ļ│¦ņØĆĻĘ╝(rectus abdominus), ļ░░Ļ░ĆļĪ£ĻĘ╝(transverse abdominus)ņØ┤ ņ׳ļŗż. ņĀüņĀłĒĢ£ ņäĖĻĖ░ņØś ĻĖ░ņ╣©ņØä ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ļéĀņł©ĻĘ╝ņ£ĪņØś Ļ░ĢĒĢ£ ņłśņČĢļ┐Éļ¦ī ņĢäļŗłļØ╝ ĻĖ░ņ╣©ņØä ĒĢśĻĖ░ ņĀäņŚÉ ļōżņł© ĻĘ╝ņ£ĪņØä ĒåĄĒĢ┤ ņČ®ļČäĒĢ£ Ļ│ĄĻĖ░ļź╝ ļōżņØ┤ņē¼ņ¢┤ņĢ╝ ĒĢ£ļŗż. ņāüĻĖ░ļÅäĻĘ╝ņ£ĪņŚÉļŖö ņØĖļæÉ(pharynx), ĒøäļæÉ(larynx), ĒśĆĻ░Ć ĒżĒĢ©ļÉśĻ│Ā, ņāüĻĖ░ļÅäļź╝ ņ£Āņ¦ĆĒĢśĻ│Ā, ņé╝Ēé¼ ļĢī ĒØĪņØĖņØ┤ ņØ╝ņ¢┤ļéśņ¦Ć ņĢŖļÅäļĪØ ĻĖ░ļÅäļź╝ ļ│┤ĒśĖĒĢśļŖö ņŚŁĒĢĀņØä ĒĢ£ļŗż[5,6].
ņłśļ®┤ ņżæņŚÉļŖö ĒśĖĒØĪĻĘ╝ņ£ĪņØś ĻĖ░ļŖźņØ┤ Ļ╣©ņ¢┤ ņ׳ņØä ļĢīļ│┤ļŗż Ļ░ÉņåīĒĢ£ļŗż. ņłśļ®┤ ņżæņŚÉļŖö ļŗżļ”¼ļćī(pons)ņÖĆ ņł©ļćī(medulla)ņŚÉ ņ׳ļŖö ĒśĖĒØĪņżæņČöĻ░Ć PaCO2ļéś pH ļ│ĆĒÖöņŚÉ ļ░śņØæĒĢśļŖö ĒÖöĒĢÖļ»╝Ļ░Éņä▒(chemosensitivity)ņØ┤ Ļ░ÉņåīĒĢśĻ│Ā, ĒśĖĒØĪņżæņČöņŚÉ ļīĆĒĢ£ ļīĆļćīĒö╝ņ¦łņØś ņ×ÉĻĘ╣ļÅä Ļ░ÉņåīĒĢ£ļŗż. ļĀśņłśļ®┤ ņżæņŚÉļŖö ĻĘ╝ņ£ĪņØś ĒÖ£ļÅÖņØ┤ Ļ░ÉņåīĒĢśļŖö ļŹ░, ņŻ╝ļĪ£ ļŹöļČĆļōżņł©ĻĘ╝ņ£Ī, Ļ░łļ╣äņé¼ņØ┤ĻĘ╝, ņāüĻĖ░ļÅäĻĘ╝ņ£ĪņØś ĒÖ£ļÅÖņØ┤ Ļ░ÉņåīĒĢśļŖö ļ░śļ®┤ ĒÜĪĻ▓®ļ¦ēņØś ĒÖ£ļÅÖņØĆ ļ│┤ņĪ┤ļÉśņ¢┤, ļĀśņłśļ®┤ ņżæņŚÉ ņØ╝ņ¢┤ļéśļŖö ĒśĖĒØĪņØĆ ļīĆļČĆļČä ĒÜĪĻ▓®ļ¦ēņŚÉ ņØśĒĢ┤ ņØ╝ņ¢┤ļé£ļŗż. ĻĘĖļ”¼Ļ│Ā ņłśļ®┤ ņżæņŚÉļŖö ņāüĻĖ░ļÅä ņĀĆĒĢŁņØ┤ ņ”ØĻ░ĆĒĢ£ļŗż[7].
ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņŚÉņä£ ĒśĖĒØĪļČĆņĀäņØĆ Ļ░ü ĒśĖĒØĪĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢ┤ņĀĖņä£ ļéśĒāĆļéśļŖö ņØ╝ļĀ©ņØś ļ│ĆĒÖöļ┐Éļ¦ī ņĢäļŗłļØ╝ ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśĻ│╝ ļÅÖļ░śļÉśļŖö ņ¦łĒÖśņØ┤ļéś ņÜöņØĖņŚÉ ņØśĒĢ┤ ņØ┤ļ»Ė ņĢĮĒĢ┤ņ¦ä ĒśĖĒØĪĻĘ╝ņ£ĪņŚÉ ļČĆļŗ┤ņØ┤ ļŹöĒĢ┤ņĀĖņä£ ņØ╝ņ¢┤ļé£ļŗż. ļōżņł©ĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢ┤ņ¦Ćļ®┤ ĒÅÉĻ░Ć ņĀ£ļīĆļĪ£ ĒīĮņ░ĮĒĢśņ¦Ć ļ¬╗ĒĢśņŚ¼ ļ»ĖņäĖļ¼┤ĻĖ░ĒÅÉ(microatelectasis)Ļ░Ć ļ░£ņāØĒĢśĻ│Ā, ĒÖśĻĖ░-Ļ┤Ćļźś ļČłĻĘĀĒśĢ(ventilation-perfusion mismatch)ņŚÉ ņØśĒĢ£ ņĀĆņé░ņåīĒśłņ”ØņØ┤ ņ£Āļ░£ļÉ£ļŗż. ļōżņł©ĻĘ╝ņ£ĪņØ┤ ļŹö ņĢĮĒĢ┤ņ¦Ćļ®┤ ņØ╝ĒÜīĒśĖĒØĪļ¤ē(tidal volume)ņØ┤ Ļ░ÉņåīĒĢśĻ▓ī ļÉśĻ│Ā, ĒśĖĒØĪņłśļź╝ ņ”ØĻ░ĆĒĢśņŚ¼ ļČäļŗ╣ ĒÖśĻĖ░ļź╝ ņ£Āņ¦ĆĒĢśļŗżĻ░Ć ņ¦ĆņåŹņĀüņØĖ ļ╣łĒśĖĒØĪņØ┤ ņØ┤ļ»Ė ņĢĮĒĢ┤ņ¦ä ĒśĖĒØĪĻĘ╝ņØś Ēö╝ļĪ£ļĪ£ ņØ┤ņ¢┤ņ¦ĆĻ│Ā, ĒÅÉĒżņĀĆĒÖśĻĖ░ņŚÉ ņØśĒĢ£ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ ļ░£ņāØĒĢ£ļŗż. ņĀĆņé░ņåīĒśłņ”ØņØĆ ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņŚÉ ņØśĒĢ£ ĒśĖĒØĪļČĆņĀäņØś ņ┤łĻĖ░ņŚÉ ļ░£ņāØĒĢśĻ│Ā, Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØĆ ĒśĖĒØĪļČĆņĀäņØ┤ ņ¦äĒ¢ēļÉśļ®┤ ļéśĒāĆļéśļŖö Ēśäņāüņ£╝ļĪ£ ņŗ¼ĒĢ£ ļōżņł©ĻĘ╝ņ£ĪņØś ņĢĮĒÖöņÖĆ Ēö╝ļĪ£ļź╝ ņØśļ»ĖĒĢ£ļŗż. ĻĘĖļ”¼Ļ│Ā ļōżņł©ĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢśņŚ¼ ĒØĪņ×ģĒĢĀ ņłś ņ׳ļŖö Ļ│ĄĻĖ░ļ¤ēņØ┤ Ļ░ÉņåīĒĢśĻ│Ā, ļéĀņł©ĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢśņŚ¼ ĻĖ░ņ╣©ņØä ĒåĄĒĢ┤ ĻĖ░ļÅäļČäļ╣äļ¼╝ņØä ņĀ£Ļ▒░ĒĢśņ¦Ć ļ¬╗ĒĢ┤ņä£ ļ¼┤ĻĖ░ĒÅÉņÖĆ ĒÅÉļĀ┤ņØś ņ£äĒŚśņØ┤ ņ”ØĻ░ĆĒĢ£ļŗż. ņāüĻĖ░ļÅäĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢśļ®┤ ļōżņł© ņżæņŚÉ ļ░£ņāØĒĢśļŖö ņØīņĢĢņ£╝ļĪ£ ņØĖĒĢ┤ ņāüĻĖ░ļÅäĒÅÉņćäĻ░Ć ņØ╝ņ¢┤ļéĀ ņłś ņ׳Ļ│Ā, ĒŖ╣Ē׳ ļłäņÜ┤ ņ×ÉņäĖņŚÉņä£ ņל ļ░£ņāØĒĢ£ļŗż. ĻĘĖļ”¼Ļ│Ā ņāüĻĖ░ļÅäĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢśļ®┤ ĒØĪņØĖņŚÉ ņØśĒĢ┤ ļ¼┤ĻĖ░ĒÅÉņÖĆ ĒÅÉļĀ┤ņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż[6,8,9].
ĒśĖĒØĪĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢ£ ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉļŖö ņłśļ®┤ņØ┤ ĒśĖĒØĪņŚÉ ļ»Ėņ╣śļŖö ņŚ¼ļ¤¼ ņśüĒ¢źņŚÉ ņØśĒĢ┤ņä£ ņłśļ®┤ ņżæņŚÉ ņĀĆĒÖśĻĖ░Ļ░Ć ņĢģĒÖöļÉśņ¢┤ ņĀĆņé░ņåīĒśłņ”ØĻ│╝ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ ņŗ¼ĒĢ┤ņ¦äļŗż. ņĢ╝Ļ░äņĀĆĒÖśĻĖ░(nocturnal hypoventilation)ļŖö ļ│┤ĒåĄ ļĀśņłśļ®┤ņŚÉņä£ ļ©╝ņĀĆ ļ░£ņāØĒĢśĻ│Ā ĒśĖĒØĪĻĘ╝ņ£ĪņØ┤ ņĀÉņ░© ņĢĮĒĢ┤ņ¦Ćļ®┤ ļ╣äļĀśņłśļ®┤Ļ│╝ ņŻ╝Ļ░äņŚÉļÅä ļéśĒāĆļé£ļŗż. ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉņŚÉņä£ ņŗ¼ĻĘ╝ļ│æņ”ØĻ│╝ ņÜĖĒśłņŗ¼ļČĆņĀäņØ┤ ļÅÖļ░śļÉśĻ▒░ļéś ļ¼┤ĻĖ░ĒÅÉļéś ĒÅÉļĀ┤ņØ┤ ļ░£ņāØĒĢśļ®┤ ņØ┤ļ»Ė ņĢĮĒĢ£ ĒśĖĒØĪĻĘ╝ņ£ĪņŚÉ ļīĆĒĢ£ ļČĆļŗ┤ņØ┤ ņ”ØĻ░ĆĒĢśņŚ¼ ĒśĖĒØĪļČĆņĀäņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ”¼Ļ│Ā Ļ▒Ęņ¦Ć ļ¬╗ĒĢśļŖö ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉļŖö Ļ╣ŖņØĆņĀĢļ¦źĒśłņĀäņ”ØņØś ņ£äĒŚśņØ┤ ņ׳Ļ│Ā, ĒÅÉņāēņĀäņ”ØņØ┤ ļ░£ņāØĒĢśņŚ¼ ĒśĖĒØĪļČĆņĀäņØś ņ£äĒŚśņØ┤ ņ”ØĻ░ĆĒĢĀ ņłś ņ׳ļŗż[3,9].
ņŗĀĻ▓ĮĻĘ╝ņ£ĪĒśĖĒØĪļČĆņĀäņØ┤ ņØśņŗ¼ļÉśļŖö ĒÖśņ×ÉņŚÉ ļīĆĒĢ£ ĒÅēĻ░ĆļŖö ņ×ÉņäĖĒĢ£ ļ│æļĀź ņ▓ŁņĘ©ļĪ£ļČĆĒä░ ņŗ£ņ×æļÉśĻ│Ā, ņ”ØņāüņØ┤ ņāłļĪ£ ņāØĻĖ┤ Ļ▓āņØĖņ¦Ć, ĻĖ░ņĪ┤ņŚÉ ņ׳ļŹś ļ¦īņä▒ĒśĖĒØĪļČĆņĀäņØ┤ ņĢģĒÖöļÉ£ Ļ▓āņØĖņ¦Ć ĒīīņĢģĒĢ£ļŗż. ņ”ØņāüņØ┤ ņŗ£ņ×æļÉ£ ņŗ£ĻĖ░, ĻĘ╝ļĀźņĢĮĒÖö ņ¢æņāü, ņ¦äĒ¢ēņåŹļÅäļź╝ ĒīīņĢģĒĢśļŖö Ļ▓āņØĆ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░Ļ░Ć ĒĢäņÜöĒĢ£ņ¦Ć ņśłņĖĪĒĢśļŖö ļŹ░ ņżæņÜöĒĢśļŗż.
ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉņŚÉņä£ ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņØ┤ ļ░£ņāØĒĢśļ®┤ ļ╣Āļź┤Ļ│Ā ņ¢ĢņØĆ ĒśĖĒØĪņØä ĒĢśĻ│Ā, ļ¼ĖņןņŚÉņä£ ļŗ©ņ¢┤ļōżņØä ņŚ░Ļ▓░ĒĢśņ¦Ć ļ¬╗ĒĢśĻ│Ā ļüŖņ¢┤ņä£ ļ¦ÉĒĢśĻ│Ā(staccato speech), Ļ░ĆļלĻ░Ć ĻĘĖļź┤ļĀüĻ▒░ļ”¼Ļ│Ā, ņé╝Ēé┤ Ļ│żļ×ĆĻ│╝ ļ░£ņä▒ņןņĢĀ(dysphonia)Ļ░Ć ļÅÖļ░śļÉ£ļŗż. ĻĘĖļ”¼Ļ│Ā ĒÖśņ×ÉļŖö Ēö╝Ļ│żĒĢ┤ ļ│┤ņØ┤Ļ│Ā ņĢłņĀłļČĆņĀłļ¬╗ĒĢśĻ│Ā, ļ¦źļ░ĢĻ│╝ ĒśĖĒØĪņØ┤ ļ╣©ļØ╝ņ¦ĆĻ│Ā, ņØ┤ļ¦łņŚÉ ļĢĆņØ┤ ļ¦║Ē׳ĻĖ░ļÅä ĒĢ£ļŗż. ĒÜĪĻ▓®ļ¦ēņØ┤ ņĢĮĒĢ┤ņä£ ļ│ĄņĢĢņØ┤ ņ”ØĻ░ĆĒĢśļŖö ņāüĒÖ®ņŚÉņä£ ĒÜĪĻ▓®ļ¦ēņØ┤ ņ£äļĪ£ ņ╣śņÜ░ņ╣Ā ļĢī ņł©ņē¼ĻĖ░Ļ░Ć ļŹö ņ¢┤ļĀżņøīņ¦ĆĻĖ░ ļĢīļ¼ĖņŚÉ, ļ¼┤Ļ▒░ņÜ┤ ļ¼╝Ļ▒┤ņØä ļōżĻ▒░ļéś ļłĢĻ▒░ļéś ļ¬ĖņØä ņĢ×ņ£╝ļĪ£ ĻĄ¼ļČĆļ”¼Ļ▒░ļéś ļ¼╝ņåŹņŚÉņä£ ĒśĖĒØĪĻ│żļ×ĆņØ┤ ņŗ¼ĒĢ┤ņ¦äļŗż. ĻĘĖļ”¼Ļ│Ā ĒÜĪĻ▓®ļ¦ēņØ┤ ņĢĮĒĢśļ®┤ ĒÖśņ×ÉļŖö ļłäņÜ┤ ņ×ÉņäĖņŚÉņä£ ĒśĖĒØĪĻ│żļ×ĆņØ┤ ņŗ¼ĒĢ┤ņĀĖņä£ ņĢēņĢäņł©ņē¼ĻĖ░(orthopnea)ļź╝ ĒĢśĻ▓ī ļÉśĻ│Ā, ĒÅēņåīņŚÉļŖö ĒśĖĒØĪĒĢĀ ļĢī ņé¼ņÜ®ĒĢśņ¦Ć ņĢŖļŖö ļ¬®Ļ░łļ╣äĻĘ╝Ļ│╝ ļ¬®ļ╣ŚĻĘ╝Ļ│╝ Ļ░ÖņØĆ ļŹöļČĆĻĘ╝ņ£ĪņØä ņé¼ņÜ®ĒĢśņŚ¼ ĒśĖĒØĪĒĢśĻ│Ā, ļōżņł©ņ£╝ļĪ£ ĒØēĻ│ĮņØ┤ ĒīĮņ░ĮļÉĀ ļĢī, ļ│ĄļČĆĻ░Ć ņĢłņ¬Įņ£╝ļĪ£ ļōżņ¢┤Ļ░ĆļŖö ņŚŁņäżĒśĖĒØĪ(paradoxical breathing)ņØ┤ ļéśĒāĆļé£ļŗż. ņŚŁņäżĒśĖĒØĪņØĆ ĒÅÉĒÖ£ļ¤ē(vital capacity)ņØ┤ ņĀĢņāüņØś 10%Ļ╣īņ¦Ć ļ¢©ņ¢┤ņ¦ä Ļ▓āņØä ņØśļ»ĖĒĢ£ļŗż. ĒÖśņ×Éļź╝ ļłĢĒśĆņä£ ņ¦äņ░░ĒĢśļ®┤ ļŹöļČĆĻĘ╝ņ£ĪņØś ņé¼ņÜ®ņØ┤ļéś ņŚŁņäżĒśĖĒØĪņØä ļŹö ņל Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ļŗż[3-6].
Ļ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉņŚÉņä£ ļ¬®ĻĄĮĒלņØś ĻĘ╝ļĀźņØĆ ĒÜĪĻ▓®ļ¦ēņØś ĻĘ╝ļĀźņØä ļ░śņśüĒĢ£ļŗż. ļ¬®ĻĄĮĒל ĻĘ╝ņ£ĪĻ│╝ ĒÜĪĻ▓®ļ¦ēņŚÉ ļÅÖņØ╝ĒĢ£ ļČäņĀłņŗĀĻ▓ĮņØ┤ ļČäĒżĒĢśĻĖ░ ļĢīļ¼ĖņØ┤ļŗż[6,10].
ņł©ļćīļ¦łļ╣äļź╝ ĒÖĢņØĖĒĢśĻĖ░ ņ£äĒĢ┤ ņ╣©ņØä ĒØśļ”¼ļŖöņ¦Ć, ņé╝ĒéżĻĖ░ ņ¢┤ļĀżņÜ┤ņ¦Ć, ņŗØĒøäĻĖ░ņ╣©ņØ┤ļéś ņ¦łņŗØņØ┤ ņ׳ļŖöņ¦Ć ļ¼╝ņ¢┤ļ│┤Ļ│Ā, ņØīņŗØņØś ĻĄ│ĻĖ░ņÖĆ Ļ│Āņ▓┤ļéś ņĢĪņ▓┤ņŚÉ ļö░ļØ╝ ņ”ØņāüņØ┤ ļŗżļźĖ ņ¦ĆļÅä ĒÖĢņØĖĒĢ£ļŗż. ĒÅÉļĀ┤ņØ┤ ņ×¼ļ░£ĒĢ£ ļ│æļĀźņØĆ ņł©ļćīļ¦łļ╣äļĪ£ ņØĖĒĢ┤ ĒØĪņØĖņØ┤ ļ░£ņāØĒĢśĻ▒░ļéś ļéĀņł©ĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢ┤ņä£ ĻĖ░ņ╣©ņØä ņĀ£ļīĆļĪ£ ĒĢśņ¦Ć ļ¬╗ĒĢśļŖö Ļ░ĆļŖźņä▒ņØä ņŗ£ņé¼ĒĢ£ļŗż. ĒÖśņ×ÉņŚÉĻ▓ī ĻĖ░ņ╣©ņØä ĒĢśļÅäļĪØ ĒĢ┤ņä£ ļōżļ”┤ ņĀĢļÅäļĪ£ ĻĖ░ņ╣©ņØä ĒĢĀ ņłś ņŚåņ£╝ļ®┤ ĻĖ░ņ╣©ņØä ĒĢśļŖö ĻĖ░ļŖźņØ┤ ļ¢©ņ¢┤ņ¦ä Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ĒĢ£ļŗż. ņé╝Ēé┤Ļ│żļ×ĆņØĆ ļ¼╝ņØä ļ¦łņŗ£ļŖö ļÅäņżæņØ┤ļéś ļ¦łņŗĀ Ēøä ĻĖ░ņ╣©ņØä ĒĢśĻ▒░ļéś ņĀ¢ņØĆ ļ¬®ņåīļ”¼ļź╝ ļé┤ļŖöņ¦Ćļź╝ Ļ▓Ćņé¼ĒĢśņŚ¼ ņäĀļ│äĒĢĀ ņłś ņ׳ļŗż[4,9].
ņł©ņØä Ļ╣ŖņØ┤ ļōżņØ┤ņē░ ņāüĒā£ņŚÉņä£ 1ņ┤łņŚÉ ņł½ņ×Éļź╝ ļæÉ Ļ░£ņö® Ēü░ņåīļ”¼ļĪ£ ņäĖĻ▓ī ĒĢśļ®┤ ņĀĢņāüņØĖņØĆ 30Ļ╣īņ¦Ć ņģĆ ņłś ņ׳ņ¦Ćļ¦ī, ĒÅÉĒÖ£ļ¤ēņØ┤ ļ¢©ņ¢┤ņ¦ä ĒÖśņ×ÉļŖö 20Ļ╣īņ¦Ć ņģĆ ņłś ņŚåĻ▓ī ļÉ£ļŗż. ļŗ©ņØ╝ĒśĖĒØĪņł½ņ×ÉņäĖĻĖ░ļŖö ĒÅÉĒÖ£ļ¤ēĻ│╝ ņĄ£ļīĆļōżņł©ņĢĢ(maximal inspiratory pressure)Ļ│╝ ņāüĻ┤ĆĻ┤ĆĻ│äĻ░Ć ņ׳ļŗż[5].
ĒÅÉĒÖ£ļ¤ēņĖĪņĀĢņØĆ ņĖĪņĀĢĻ░Æ ņ×Éņ▓┤ļ│┤ļŗżļŖö ņŗ£Ļ░äņŚÉ ļö░ļźĖ ņĖĪņĀĢĻ░ÆņØś ļ│ĆĒÖöĻ░Ć ļŹö ņżæņÜöĒĢśļ®░, ļ¦żļ▓ł Ļ░ÖņØĆ ņ×ÉņäĖņŚÉņä£ ņĖĪņĀĢĒĢ┤ņĢ╝ ĒĢ£ļŗż. Ļ▓Ćņé¼ĒĢĀ ļĢī Ļ│ĄĻĖ░Ļ░Ć ņāłņ¦Ć ņĢŖļÅäļĪØ ĒĢśĻ│Ā, 3ĒÜī ņŗ£Ē¢ēĒĢśņŚ¼ Ļ░Ćņן ļåÆņØĆ ņĖĪņĀĢĻ░ÆņØä ņé¼ņÜ®ĒĢ£ļŗż. Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ē(forced vital capacity), ņĄ£ļīĆļōżņł©ņĢĢ, ņĄ£ļīĆļéĀņł©ņĢĢņØĆ ĒśĖĒØĪĻĖ░ļŖźņØä ĒÅēĻ░ĆĒĢśĻĖ░ ņ£äĒĢ┤ Ļ░Ćņן ļäÉļ”¼ ņé¼ņÜ®ļÉśļŖö ņ¦ĆĒæ£ņØ┤ļŗż. ņĀĢņāü ņä▒ņØĖņØś ĒÅÉĒÖ£ļ¤ēņØĆ 60-70 mL/kgņØ┤Ļ│Ā, Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ēņØ┤ 20 mL/kg ļ»Ėļ¦īņØ┤Ļ▒░ļéś, 1 L ļ»Ėļ¦īņØ┤Ļ▒░ļéś, 24ņŗ£Ļ░ä ļÅÖņĢł 30% ņØ┤ņāü Ļ░ÉņåīĒĢśļŖö Ļ▓āņØĆ ĒśĖĒØĪļČĆņĀäņØ┤ ņ×äļ░ĢĒĢ£ ņ¦ĆĒæ£ņØ┤ļŗż. ņĢēņØĆ ņ×ÉņäĖņŚÉ ļ╣äĒĢ┤ ļłäņÜ┤ ņ×ÉņäĖņŚÉņä£ Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ēņØ┤ 20% ļäśĻ▓ī Ļ░ÉņåīĒĢśļŖö Ļ▓āņØĆ ĒÜĪĻ▓®ļ¦ēņØ┤ ņĢĮĒĢśļŗżļŖö Ļ▓āņØä ņØśļ»ĖĒĢ£ļŗż. ŌĆś20-30-40 ļ▓Ģņ╣ÖŌĆÖņØĆ Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ē 20 mL/kg ļ»Ėļ¦ī, ņĄ£ļīĆļōżņł©ņĢĢ 30 cmH2O ļ»Ėļ¦ī, ņĄ£ļīĆļéĀņł©ņĢĢ 40 cmH2O ļ»Ėļ¦īņØ┤ļ®┤ ĒÖśņ×ÉĻ░Ć ĒśĖĒØĪļČĆņĀäņØś ņ£äĒŚśņØ┤ ņ׳ļŖö Ļ▓āņ£╝ļĪ£ Ļ░äņŻ╝ĒĢśĻ│Ā ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņŗ£Ē¢ēĒĢśļŖö Ļ▓āņØ┤ļŗż[3,5,11]. ņ¢╝ĻĄ┤ļ¦łļ╣äĻ░Ć ņ׳ņ£╝ļ®┤ ņ×ģņ£╝ļĪ£ ļ░öļ×īņØ┤ ņāłņ¢┤ ļéśĻ░Ćņä£ Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ē, ņĄ£ļīĆļōżņł©ņĢĢ, ņĄ£ļīĆļéĀņł©ņĢĢņØ┤ ņŗżņĀ£ļ│┤ļŗż ļé«Ļ▓ī ņĖĪņĀĢļÉĀ ņłś ņ׳ļŗż. Sniff nasal inspiratory pressure (SNIP)ļŖö ņØ┤ Ļ▓ĮņÜ░ņŚÉ ļÅäņøĆņØ┤ ļÉśļŖö ņ¦ĆĒæ£ļĪ£ņŹ© ĒĢ£ņ¬Į ņĮ¦ĻĄ¼ļ®Źņ£╝ļĪ£ ņł©ņØä ļōżņØ┤ņē┤ ļĢī ļ¦ēĒ×ī ļ░śļīĆņ¬Į ņĮ¦ĻĄ¼ļ®ŹņŚÉņä£ ņĢĢļĀźņØä ņĖĪņĀĢĒĢ£ļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ SNIPņØ┤ ņĄ£ļīĆļōżņł©ņĢĢļ│┤ļŗż Ēü¼ļŗż[5,11].
ņĄ£ļīĆĻĖ░ņ╣©ņ£Āļ¤ē(peak cough flow)ņØĆ ĒÜ©ņ£©ņĀüņØĖ ĻĖ░ļÅäļČäļ╣äļ¼╝ ņĀ£Ļ▒░ļź╝ ļ░śņśüĒĢśļŖö ņ¦ĆĒæ£ļĪ£ņŹ© ņĄ£ļīĆņ£Āļ¤ēĻ│ä(peak flow meter)ļź╝ ĒåĄĒĢ┤ ņĄ£ļīĆĒĢ£ Ēלņ░©Ļ▓ī ĻĖ░ņ╣©ņØä ĒĢśļÅäļĪØ ĒĢśņŚ¼ ņĖĪņĀĢĒĢ£ļŗż. ņĀĢņāü ņä▒ņØĖņØś ņĄ£ļīĆĻĖ░ņ╣©ņ£Āļ¤ēņØĆ 360-840 L/minņØ┤Ļ│Ā 160 L/min ņØ┤ņāüņØ┤ņ¢┤ņĢ╝ ĻĖ░ļÅäņŚÉņä£ ļČäļ╣äļ¼╝ņØ┤ļéś ņØ┤ļ¼╝ņ¦ł ļō▒ņØä ņĀ£Ļ▒░ĒĢĀ ņłś ņ׳ļŗż[11].
ĒÅÉĒżņŚÉņä£ ĒÅÉļ¬©ņäĖĒśłĻ┤Ćņ£╝ļĪ£ ĒÖĢņé░ļÉśļŖö ņé░ņåīļŖö ņĢĮ 98%Ļ░Ć ņĀüĒśłĻĄ¼ņØś ĒśłņāēņåīņÖĆ Ļ▓░ĒĢ®ĒĢ£ļŗż. ņé░ņåīĻ░Ć Ļ▓░ĒĢ®ĒĢ£ ņé░ņåīĒśłņāēņåīņØś ļ░▒ļČäņ£©ņØĆ ņé░ņåīĒżĒÖöļÅäļź╝ ņĖĪņĀĢĒĢśņŚ¼ ņĢī ņłś ņ׳ļŗż. SaO2ļŖö ļÅÖļ¦źĒśłņŚÉņä£ ņé░ņåīĒżĒÖöļÅäļź╝ ņĖĪņĀĢĒĢśļŖö Ļ▓āņØ┤Ļ│Ā SpO2ļŖö ļ¦źļ░Ģņé░ņåīņĖĪņĀĢņØä ĒåĄĒĢ┤ ļ¬©ņäĖĒśłĻ┤Ćļ░öĒāĢ(capillary bed)ņŚÉņä£ ņé░ņåīĒżĒÖöļÅäļź╝ ļ╣äņ╣©ņŖĄņĀüņ£╝ļĪ£ ņČöņĀĢĒĢśļŖö Ļ░ÆņØ┤ļŗż. SpO2ļŖö SaO2ņÖĆ ņāüĻ┤ĆĻ┤ĆĻ│äĻ░Ć ļåÆņ¦Ćļ¦ī SaO2Ļ░Ć 90% ļ»Ėļ¦īņØ┤ļ®┤ ņĀĢĒÖĢļÅäĻ░Ć ļ¢©ņ¢┤ņ¦äļŗż. ĻĘĖļ”¼Ļ│Ā ļ¦źļ░Ģņé░ņåīņĖĪņĀĢņØĆ ĒÖśņ×ÉņØś ņøĆņ¦üņ×ä, ņĀĆĒśłņĢĢņØ┤ļéś ņ▓┤ņś©ņĀĆĒĢśņŚÉ ļö░ļźĖ Ļ┤ĆļźśņĀĆĒĢś, ļ╣łĒśł, ļ®öĒŖĖĒśłņāēņåīĒśłņ”ØņØ┤ļéś ņØ╝ņé░ĒÖöĒāäņåīņżæļÅģ ļō▒ņØś ņśüĒ¢źņ£╝ļĪ£ ņĀĢĒÖĢļÅäĻ░Ć ļ¢©ņ¢┤ņ¦ł ņłś ņ׳ļŗż. PaO2ļŖö ĒÅÉĒżņŚÉņä£ ĒÅÉļ¬©ņäĖĒśłĻ┤Ćņ£╝ļĪ£ ĒÖĢņé░ļÉśņ¢┤ Ēśłņןņ£╝ļĪ£ ņÜ®ĒĢ┤ļÉśļŖö ņĢĮ 2%ņØś ņé░ņåīļź╝ ļ░śņśüĒĢśĻ│Ā ļÅÖļ¦źĒśłĻĖ░ņ▓┤ņŚÉņä£ ņĖĪņĀĢĒĢ£ļŗż. PaO2/FiO2ļŖö ņé░ņåīĒÖöļź╝ ņĖĪņĀĢĒĢśļŖö ļśÉļŗżļźĖ ņ▓ÖļÅäņØ┤ļŗż. FiO2ļŖö ļōżņł©ņé░ņåīļČäņ£©ļĪ£ ņŗżļé┤ Ļ│ĄĻĖ░ņØś FiO2ļŖö 0.21ņØ┤ļŗż. PaO2/FiO2 ņĀĢņāüļ▓öņ£äļŖö 300-500 mmHgņØ┤Ļ│Ā 300 mmHg ļ»Ėļ¦īņØĆ ņĀĆņé░ņåīĒśłņ”ØņØä ņØśļ»ĖĒĢ£ļŗż[12,13].
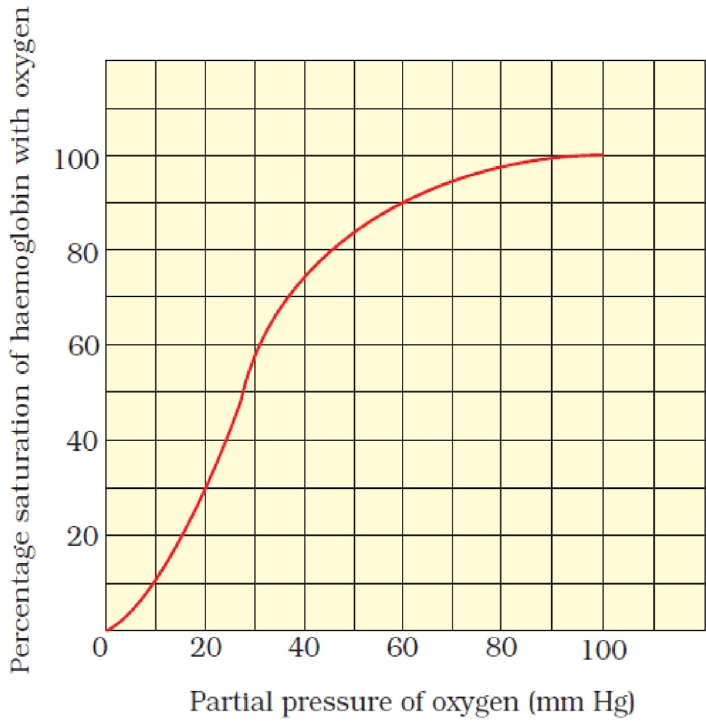
ļ¦źļ░Ģņé░ņåīņĖĪņĀĢņØĆ PaO2ļź╝ ņĖĪņĀĢĒĢśļŖö Ļ▓āņØ┤ ņĢäļŗłļ»ĆļĪ£ ļ¦źļ░Ģņé░ņåīņĖĪņĀĢņŚÉ ņ¦Ćļéśņ╣śĻ▓ī ņØśņĪ┤ĒĢśļ®┤ ņ×äņāüņĀüņ£╝ļĪ£ ņżæņÜöĒĢ£ ņĀĆņé░ņåīĒśłņ”ØņØä ļåōņ╣Ā ņłś ņ׳ļŗż. ņé░ņåīĒśłņāēņåīĒĢ┤ļ”¼Ļ│ĪņäĀņØś Ļ░ĆĒīīļźĖ ļČĆļČäņØĖ PaO2Ļ░Ć ņĢĮ 60-70 mmHgņŚÉ ļÅäļŗ¼ĒĢĀ ļĢīĻ╣īņ¦ĆļŖö PaO2Ļ░Ć ļ¦ÄņØ┤ ļ¢©ņ¢┤ņĀĖļÅä ņé░ņåīĒżĒÖöļÅäņØś Ļ░ÉņåīļŖö Ēü¼ņ¦Ć ņĢŖĻ│Ā(Fig. 1) ļ¦źļ░Ģņé░ņåīņĖĪņĀĢņØĆ ļ¬ć ņ┤łĻ░äņØś ĒÅēĻĘĀņŗĀĒśĖņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ ņĀĆņé░ņåīĒśłņ”ØņØ┤ ļ░£ņāØĒĢ£ Ēøä Ļ▒░ņØś 1ļČä ļÅÖņĢł ņĀĆņé░ņåīĒśłņ”ØņØä Ļ░Éņ¦ĆĒĢśņ¦Ć ļ¬╗ĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ”¼Ļ│Ā ļ¦źļ░Ģņé░ņåīņĖĪņĀĢņØĆ ņé░ņåīĒżĒÖöļÅäļź╝ ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŖö ĒÄĖļ”¼ĒĢ£ ļ░®ļ▓ĢņØ┤ņ¦Ćļ¦ī, ĒÖśĻĖ░ņØś ņ¦ĆĒæ£ņØĖ PaCO2ļź╝ ņĖĪņĀĢĒĢśņ¦Ć ļ¬╗ĒĢ£ļŗż[11].
ņŗĀĻ▓ĮĻĘ╝ņ£ĪĒśĖĒØĪļČĆņĀä ņ┤łĻĖ░ņŚÉļŖö ļ¼┤ĻĖ░ĒÅÉņŚÉ ņØśĒĢ┤ PaO2Ļ░Ć Ļ░ÉņåīĒĢśĻ│Ā ĒøäĻĖ░ņŚÉļŖö ĒÅÉĒżņĀĆĒÖśĻĖ░ņŚÉ ņØśĒĢ┤ PaCO2Ļ░Ć ņ”ØĻ░ĆĒĢśļŖö ņĀĆņé░ņåīĒśłņ”ØĻ│╝ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ Ēś╝ĒĢ®ļÉ£ ĒśĖĒØĪļČĆņĀäņØ┤ ņØ╝ņ¢┤ļé£ļŗż. PaCO2ļŖö ĒÜĪĻ▓®ļ¦ēņØ┤ ņĢĮĒĢ┤ņ¦ÉņŚÉ ļö░ļØ╝ ņĀÉņ░© ņ”ØĻ░ĆĒĢ£ļŗż. ĒśĖĒØĪņłśĻ░Ć ņ”ØĻ░ĆĒĢ©ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā PaCO2Ļ░Ć ņĀĢņāüņØĖ Ļ▓ĮņÜ░ļÅä ņ¢ĢņØĆ ĒśĖĒØĪņ£╝ļĪ£ ņØĖĒĢ┤ ĒÖśĻĖ░Ļ░Ć ņĀ£ļīĆļĪ£ ņØ┤ļŻ©ņ¢┤ņ¦Ćņ¦Ć ņĢŖļŖöļŗżļŖö Ļ▓āņØä ņØśļ»ĖĒĢśļ»ĆļĪ£ ĒśĖĒØĪļČĆņĀäņØä ņØśņŗ¼ĒĢ┤ņĢ╝ ĒĢśļŖö ņåīĻ▓¼ņØ┤ļŗż[5,6].
ņŗĀĻ▓ĮĻĘ╝ņ£ĪĒśĖĒØĪļČĆņĀäņŚÉņä£ļŖö ņĀĆĒÖśĻĖ░ņŚÉ ņØśĒĢ┤ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ ļ░£ņāØĒĢśĻ│Ā pHĻ░Ć Ļ░ÉņåīĒĢśļ®┤ ĒśĖĒØĪņżæņČöĻ░Ć ņ×ÉĻĘ╣ļÉśņ¢┤ ĒśĖĒØĪņØ┤ ņ£Āļ░£ļÉśĻ│Ā ņ▓┤ļé┤ņØś ņØ┤ņé░ĒÖöĒāäņåīĻ░Ć ļ░░ņČ£ļÉśņ¦Ćļ¦ī, ņĀĆĒÖśĻĖ░ ņāüĒā£Ļ░Ć 24-48ņŗ£Ļ░ä ņØ┤ņāü ņ¦ĆņåŹļÉśļ®┤ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ ņ׳ļŹöļØ╝ļÅä ņŗĀņןņØś ļ│┤ņāüņ×æņÜ®ņ£╝ļĪ£ pHĻ░Ć ņżæĒÖöļÉśņ¢┤ ĒśĖĒØĪņżæņČöļŖö ļŹö ņØ┤ņāü ņ×ÉĻĘ╣ļÉśņ¦Ć ņĢŖĻ│Ā PaO2ņŚÉ ļö░ļØ╝ ĒśĖĒØĪņżæņČöĻ░Ć ņ×ÉĻĘ╣ļÉ£ļŗż. ņØ┤ļ¤░ ņāüĒā£ņŚÉņä£ ĒÖśĻĖ░ļ│┤ņĪ░ ņŚåņØ┤ ņé░ņåīļź╝ Ļ│ĄĻĖēĒĢśļ®┤ ĒÖśņ×ÉņØś ĒśĖĒØĪņØĆ ļŹöņÜ▒ ņĢĮĒĢ┤ņĀĖņä£ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ ņĢģĒÖöļÉ£ļŗż. ļö░ļØ╝ņä£ ĒÖśĻĖ░ņןņĢĀĻ░Ć ņØśņŗ¼ļÉśļŖö ĒÖśņ×ÉņŚÉņä£ ņé░ņåīĒżĒÖöļÅäĻ░Ć ņĀĆĒĢśļÉśļŹöļØ╝ļÅä ņé░ņåīļź╝ ļ©╝ņĀĆ Ļ│ĄĻĖēĒĢĀ Ļ▓āņØ┤ ņĢäļŗłļØ╝ ņĀĆĒÖśĻĖ░ļĪ£ ņØĖĒĢ£ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”Ø ņ£Āļ¼┤ļź╝ ĒÖĢņØĖĒĢśņŚ¼ ĒÖśĻĖ░ļź╝ ņĀüņĀłĒĢśĻ▓ī ļ│┤ņĪ░ĒĢ┤ņĢ╝ ĒĢ£ļŗż[11].
ĒÖśĻĖ░ļ│┤ņĪ░ņŚÉļŖö ļ¦łņŖżĒü¼ļź╝ ņØ┤ņÜ®ĒĢśļŖö ļ╣äņ╣©ņŖĄĒÖśĻĖ░ņÖĆ ĻĖ░Ļ┤Ć ļé┤ ņéĮĻ┤ĆņØ┤ļéś ĻĖ░Ļ┤ĆņĀłĻ░£ļź╝ ĒåĄĒĢ£ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░Ļ░Ć ņ׳ļŗż. ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņØ┤ ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņŚÉņä£ ļ░£ņāØĒĢśĻ│Ā, ĒÅÉĒżņĀĆĒÖśĻĖ░Ļ░Ć ņŻ╝ņÜö ņøÉņØĖņØ┤Ļ│Ā ĻĖ░ļÅäļČäļ╣äļ¼╝ņØä Ļ┤Ćļ”¼ĒĢĀ ņłś ņ׳Ļ│Ā ņØśņŗØņØ┤ ņĀĢņāüņØ┤ļØ╝ļ®┤ ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļź╝ ņŗ£Ē¢ēĒĢ£ļŗż. ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉņŚÉņä£ ļ¦ÄņØ┤ ņé¼ņÜ®ĒĢśļŖö ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļŖö ņØ┤ņāüĻĖ░ļÅäņ¢æņĢĢ(bilevel positive airway pressure, BiPAP)ņØ┤ļŗż. ĻĘĖļ¤¼ļéś ĻĖ░ļÅäļČäļ╣äļ¼╝ņØä Ļ┤Ćļ”¼ĒĢĀ ņłś ņŚåĻ▒░ļéś ņØ╝ņĀĢĻĖ░Ļ░ä ļé┤ņŚÉ ĒÜīļ│ĄļÉśĻĖ░ ņ¢┤ļĀżņÜ┤ ņŗ¼ĒĢ£ ņĀĆņé░ņåīĒśłņ”ØĻ│╝ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ ņ׳Ļ▒░ļéś ņØśņŗØņןņĢĀļéś ņŗ¼ĒĢ£ ņØĖņ¦ĆņןņĢĀĻ░Ć ņ׳ņ£╝ļ®┤ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņŗ£ņ×æĒĢ┤ņĢ╝ ĒĢ£ļŗż. ņéĮĻ┤ĆņØ┤ ļŖ”ņ¢┤ņ¦Ćļ®┤ ņŗ¼ĒÅÉņĀĢņ¦ĆĻ░Ć ļ░£ņāØĒĢĀ ņłś ņ׳Ļ│Ā ņØæĻĖēņéĮĻ┤Ć(emergency intubation)ņØä ĒĢśĻ▓ī ļÉśļ®┤ ĒØĪņØĖĻ│╝ ņĀĆņé░ņåīĒśłņ”Ø ļō▒ņØś ĒĢ®ļ│æņ”Ø ņ£äĒŚśņØ┤ Ēü¼Ļ▓ī ņ”ØĻ░ĆĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņéĮĻ┤ĆĻ│╝ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░Ļ░Ć ĒĢäņÜöĒĢ£ ĒÖśņ×Éļź╝ ņśłņĖĪĒĢśĻ│Ā ņäĀļ│äĒĢ┤ņä£ ņśłņĀĢņéĮĻ┤ĆņØä ņ¦äĒ¢ēĒĢśļŖö Ļ▓āņØ┤ ļ░öļ×īņ¦üĒĢśļŗż[11,14]. ĻĖ░Ļ│äĒÖśĻĖ░Ļ░Ć 3ņŻ╝ ņØ┤ņāü ņśłņāüļÉśļŖö Ļ▓ĮņÜ░ ĻĖ░Ļ┤ĆņĀłĻ░£ļź╝ Ļ│ĀļĀżĒĢ┤ņĢ╝ ĒĢ£ļŗż. ņĪ░ĻĖ░ņŚÉ ĻĖ░Ļ┤ĆņĀłĻ░£ļź╝ ĒĢĀ Ļ▓ĮņÜ░ ĒÖśņ×ÉĻ░Ć ĒÄĖĒĢśĻ│Ā ĻĄ¼Ļ░Ģņ£äņāØĻ│╝ ņåīĒåĄņØ┤ ņÜ®ņØ┤ĒĢśļŗżļŖö ņןņĀÉņØ┤ ņ׳ļŗż. ĻĖ░Ļ┤ĆņĀłĻ░£Ļ░Ć ņ¦ĆņŚ░ļÉśļ®┤ ĒÖśĻĖ░Ļ┤ĆļĀ©ĒÅÉļĀ┤ņØś ņ£äĒŚśņØ┤ ņ”ØĻ░ĆĒĢśĻ│Ā ĒøäļæÉņŗĀĻ▓Į, ĒøäļæÉņĀÉļ¦ē, ņä▒ļīĆĻ░Ć ņåÉņāüļÉśĻ▒░ļéś ņāøĻĖĖ(fistula)ņØ┤ ļ░£ņāØĒĢĀ ņ£äĒŚśņØ┤ ņ”ØĻ░ĆĒĢ£ļŗż[15].
ļ¦īņä▒ ņŗĀĻ▓ĮĻĘ╝ņ£ĪĒśĖĒØĪļČĆņĀä ĒÖśņ×É ņżæ ĻĖ░ļÅäļČäļ╣äļ¼╝ņØ┤ ļ¦ÄĻ▒░ļéś ļ╣äņ╣©ņŖĄĒÖśĻĖ░ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ĒśĖĒØĪļČĆņĀäņØ┤ ņ¦äĒ¢ēĒĢśĻ│Ā, ņāØļ¬ģņŚ░ņןņØä ņøÉĒĢśļŖö ĒÖśņ×ÉļŖö ĻĖ░Ļ┤ĆņĀłĻ░£ļź╝ ĒåĄĒĢ£ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņŗ£Ē¢ēĒĢ£ļŗż. ĻĖ░Ļ┤ĆņĀłĻ░£ļź╝ ĒĢśļ®┤ ļ¦ÉĒĢśĻĖ░ņÖĆ ņé╝Ēé┤ņןņĢĀĻ░Ć ļ░£ņāØĒĢśĻ│Ā, ĻĖ░ļÅäĻ░Ć ņ×ÉĻĘ╣ļÉśņ¢┤ ĻĖ░ļÅäļČäļ╣äļ¼╝ņØ┤ ņ”ØĻ░ĆĒĢśĻ│Ā, ĒśĖĒØĪĻĖ░Ļ░ÉņŚ╝ņØś ļ╣łļÅäĻ░Ć ņ×”ņĢäņ¦äļŗż[4,16].
ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉņŚÉņä£ ĒśĖĒØĪĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢ┤ņĀĖņä£ ĻĖ░ņ╣©ņØä ņל ĒĢśņ¦Ć ļ¬╗ĒĢśļ®┤ ĻĖ░ļÅäļČäļ╣äļ¼╝ņØ┤ ĒÜ©ņ£©ņĀüņ£╝ļĪ£ ņÖĖļČĆļĪ£ ļ░░ņČ£ļÉśņ¦Ć ļ¬╗ĒĢśņŚ¼ ļ¼┤ĻĖ░ĒÅÉņÖĆ ĒÅÉļĀ┤ ļō▒ņØś ĒĢ®ļ│æņ”ØņØ┤ ņ£Āļ░£ļÉ£ļŗż. ņĀĢņ▓┤ļÉ£ ĻĖ░ļÅä ļČäļ╣äļ¼╝ņØä ņĀ£Ļ▒░ĒĢśļ®┤ ĒśĖĒØĪĒĢĀ ļĢī ĒśĖĒØĪĻĘ╝ņ£ĪņØś ļČĆļŗ┤ņØ┤ ņżäĻ│Ā, ĒśĖĒØĪņØ┤ Ē¢źņāüļÉśļ®░, ĒśĖĒØĪĻĖ░ĒĢ®ļ│æņ”ØņØä ņśłļ░®ĒĢśĻ│Ā, ņØ┤ļ»Ė ļ░£ņāØĒĢ£ ĒśĖĒØĪĻĖ░ĒĢ®ļ│æņ”ØņØ┤ ļ╣©ļ”¼ ĒÜīļ│ĄļÉśļŖö ļŹ░ ļÅäņøĆņØ┤ ļÉ£ļŗż. ļÅäņłśļ│┤ņĪ░ĻĖ░ņ╣©(manually assisted cough)Ļ│╝ ĻĖ░ņ╣©ņ£Āļ░£ĻĖ░(mechanical insufflation-exsufflation)ļź╝ ĒåĄĒĢ┤ ĻĖ░ļÅäļČäļ╣äļ¼╝ņØä ņĀ£Ļ▒░ĒĢĀ ņłś ņ׳ļŗż[11].
ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņŚÉņä£ ĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņżæļŗ©ĒĢśĻĖ░ ņ£äĒĢ£ ĻĖ░ņżĆņØĆ ĻĖ░ņ╣©ņ£Āļ░£ĻĖ░ļĪ£ ĒśĖĒØĪļČäļ╣äļ¼╝ņØä ņĀ£Ļ▒░ĒĢĀ ņłś ņ׳Ļ│Ā, ņé░ņåīļź╝ Ēł¼ņŚ¼ĒĢśņ¦Ć ņĢŖĻ▒░ļéś ņé░ņåīļź╝ Ēł¼ņŚ¼ĒĢĀ Ļ▓ĮņÜ░ FiO2 40% ņØ┤ĒĢśņŚÉņä£ ņé░ņåīĒżĒÖöļÅäĻ░Ć 94% ņØ┤ņāüņØ┤Ļ│Ā, ĒØēļČĆņśüņāüņŚÉņä£ ĒÅÉļĀ┤ņØ┤ ĒśĖņĀäļÉśĻ│Ā, ĒÖśņ×ÉņØś ņŗ¼ĒÅÉņāüĒā£Ļ░Ć ņĢłņĀĢļÉśĻ│Ā, ņØĖņ¦ĆņןņĢĀĻ░Ć ņŚåņ¢┤ņĢ╝ ĒĢ£ļŗż[14].
ĻĖ░Ļ│äĒÖśĻĖ░ņØś ņżæļŗ©ņØĆ 3ļŗ©Ļ│äļź╝ Ļ▒░ņ│É ņØ┤ļŻ©ņ¢┤ņ¦ĆļŖö ļŹ░, ĒÖśĻĖ░ļ│┤ņĪ░ļź╝ ņĀÉņ░© ņżäņŚ¼ņä£ ĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņżæļŗ©ĒĢĀ ņżĆļ╣äĻ░Ć ļÉśņŚłļŖöņ¦Ć ĒīÉļŗ©ĒĢśĻ│Ā(readiness assessment), ņ×Éļ░£ĒśĖĒØĪņØ┤ Ļ░ĆļŖźĒĢ£ņ¦Ć ĒÖĢņØĖĒĢ£ Ēøä(spontaneous breathing trial), Ļ┤ĆņØä ņĀ£Ļ▒░ĒĢ£ļŗż. ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉļŖö ĒśĖĒØĪĻĘ╝ņ£ĪņØ┤ ņĢĮĒĢ┤ņä£ Ļ┤ĆņØä ņĀ£Ļ▒░ĒĢśļŖö ļŹ░ ņŗżĒī©ĒĢśļŖö Ļ▓ĮņÜ░Ļ░Ć 27-48%ļĪ£ ĒØöĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ ņżæļŗ©ņØä Ļ│ĀļĀżĒĢĀ ļĢī Ļ░üļ│äĒĢ£ ņŻ╝ņØśĻ░Ć ĒĢäņÜöĒĢśļŗż. ņ×Éļ░£ĒśĖĒØĪņŗ£ļÅäļź╝ 30ļČä ņØ┤ņāü ņŗ£Ē¢ēĒĢśĻĖ░ļÅä ĒĢśĻ│Ā, Ļ┤ĆņØä ņĀ£Ļ▒░ĒĢ£ ĒøäņŚÉ ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņĀĆĒÖśĻĖ░ļź╝ ļ│┤ņĪ░ĒĢĀ ņłś ņ׳ļŗż[14,17].
ĒśĖĒØĪļČĆņĀäņØĆ ĻĖ░ņ¢Ł-ļ░öļĀłņ”ØĒøäĻĄ░ņØś Ļ░Ćņן ņŗ¼Ļ░üĒĢ£ ĒĢ®ļ│æņ”Øņ£╝ļĪ£ 20-30% ĒÖśņ×ÉņŚÉņä£ ļ░£ņāØĒĢ£ļŗż. ĻĘ╝ļĀźņĀĆĒĢśĻ░Ć ļ╣Āļź┤Ļ▓ī ņ¦äĒ¢ēĒĢĀ ļĢī, ļČĆņĀĢļ¦źņØ┤ļéś ņŗ¼ĒĢ£ ĒśłņĢĢļ│ĆĒÖö Ļ░ÖņØĆ ņŗ¼ĒśłĻ┤Ćņ×Éņ£©ņŗĀĻ▓Į ĻĖ░ļŖźņןņĢĀĻ░Ć ņŗ¼ĒĢĀ ļĢī, ņé╝Ēé┤ņןņĢĀĻ░Ć ņŗ¼ĒĢĀ ļĢī, ņ¦äĒ¢ēĒĢśļŖö ĒśĖĒØĪĻ│żļ×Ć, Erasmus GBS Respiratory Insufficiency Score (EGRIS) ņĀÉņłśĻ░Ć 4ņĀÉņØä ļäśņ£╝ļ®┤ ņżæĒÖśņ×ÉņŗżņŚÉ ņ×ģņøÉĒĢ┤ņĢ╝ ĒĢ£ļŗż. EGRIS ņĀÉņłśļŖö ĒÅēĻ░Ć 1ņŻ╝ ņØ┤ļé┤ņŚÉ ĻĖ░Ļ│äĒÖśĻĖ░Ļ░Ć ĒĢäņÜöĒĢĀ ĒÖĢļźĀņØä Ļ│äņé░ĒĢ£ļŗż(Table 1) [18].
ĒśĖĒØĪĻ│żļ×ĆņØ┤ ņ׳ļŖö ĒÖśņ×ÉņŚÉņä£ ļé«ņŚÉļŖö 2-4ņŗ£Ļ░äļ¦łļŗż, ļ░żņŚÉļŖö 4-6ņŗ£Ļ░äļ¦łļŗż Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ē, ņĄ£ļīĆļōżņł©ņĢĢ, ņĄ£ļīĆļéĀņł©ņĢĢņØä ņĖĪņĀĢĒĢ£ļŗż. ĻĖ░ņ¢Ł-ļ░öļĀłņ”ØĒøäĻĄ░ņØĆ ĒÜīļ│ĄĒĢśļŖö ļŹ░ ņŗ£Ļ░äņØ┤ ļ¦ÄņØ┤ Ļ▒ĖļĀżņä£ ņןĻĖ░Ļ░ä ĒÖśĻĖ░ļ│┤ņĪ░Ļ░Ć ĒĢäņÜöĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļ│┤ļŗż ņéĮĻ┤ĆĻ│╝ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņŗ£Ē¢ēĒĢśļŖö Ļ▓āņØ┤ ĻČīņןļÉ£ļŗż. ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļŖö ņśżĒ׳ļĀż ņØæĻĖēņéĮĻ┤ĆņØś ņ£äĒŚśņØä ņ”ØĻ░Ćņŗ£ĒéżĻ│Ā ņ×Éņ£©ņŗĀĻ▓Į ĻĖ░ļŖźņןņĢĀļź╝ ņĢģĒÖöņŗ£Ēé¼ ņłś ņ׳ļŗż[5,6,9,15].
ĻĖ░ņ¢Ł-ļ░öļĀłņ”ØĒøäĻĄ░ ĒÖśņ×ÉļŖö ĒÜīļ│Ąļŗ©Ļ│äņŚÉņä£ ņŗ¼ĒśłĻ┤ĆĻ│╝ ĒśĖĒØĪ ĻĖ░ļŖźņןņĢĀļĪ£ ņé¼ļ¦ØĒĢĀ ņłś ņ׳ļŗż. ņżæĒÖśņ×ÉņŗżņŚÉņä£ ņØ╝ļ░śļ│æņŗżļĪ£ ņś«ĻĖ┤ Ēøä ņØ╝ņĀĢĻĖ░Ļ░ä ļČĆņĀĢļ¦ź, ĒśłņĢĢļ│ĆĒÖö, ĒśĖĒØĪĻ│żļ×ĆņŚÉ ļīĆĒĢ£ Ļ░Éņŗ£ļź╝ ņ¦ĆņåŹĒĢśĻ│Ā, ĒŖ╣Ē׳ ņŗ¼ĒśłĻ┤Ć ņ£äĒŚśņØĖņ×ÉĻ░Ć ņ׳ļŖö ĒÖśņ×ÉļŖö ļŹö ņŻ╝ņØśĒĢ£ļŗż[18].
ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Øņ£äĻĖ░ļŖö ņĀäņŗĀ ĻĘ╝ļĀźņĢĮĒÖöĻ░Ć ņŗ¼ĒĢ┤ņ¦Ćļ®┤ņä£ ĒśĖĒØĪļČĆņĀäņØ┤ ļÅÖļ░śļÉ£ ņāüĒā£ļĪ£, ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Ø ĒÖśņ×É ņĢĮ 15-20%ņŚÉņä£ ļ░£ņāØĒĢśĻ│Ā, ļīĆļČĆļČä ņ”Øņāü ļ░£ņāØ 1ļģä ņØ┤ļé┤ņŚÉ ņāØĻĖ┤ļŗż. ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Øņ£äĻĖ░ļŖö ņ¦łļ│æņ×Éņ▓┤ļ┐Éļ¦ī ņĢäļŗłļØ╝, Ļ│ĀņÜ®ļ¤ē ņŖżĒģīļĪ£ņØ┤ļō£ņ╣śļŻī, ņŗĀĻ▓ĮĻĘ╝ņ£ĪņĀäļŗ¼ņŚÉ ņśüĒ¢źņØä ņŻ╝ļŖö ņĢĮ, Ļ░ÉņŚ╝, ņ×äņŗĀ, ņłśņłĀ ļō▒ņŚÉ ņØśĒĢ┤ ņ£Āļ░£ļÉĀ ņłś ņ׳ļŗż[5,9,19].
ļīĆļČĆļČäņØś ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Øņ£äĻĖ░ļŖö ņé¼ņĀäņŚÉ ņśłņĖĪņØ┤ Ļ░ĆļŖźĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░ņŻ╝ņé¼ļéś ĒśłņןĻĄÉĒÖśņłĀļĪ£ ņśłļ░®ĒĢĀ ņłś ņ׳Ļ│Ā, ņłśņłĀ Ēøä ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Øņ£äĻĖ░ņØś ņ£äĒŚśņØ┤ ļåÆņØĆ ĒÖśņ×ÉņŚÉņä£ļŖö ņłśņłĀ ņĀäņŚÉ ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░ņŻ╝ņé¼ļéś ĒśłņןĻĄÉĒÖśņłĀņØä ņŗ£Ē¢ēĒĢ£ļŗż. ņłśņłĀ Ēøä ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Øņ£äĻĖ░ļŖö ņ”ØņāüņØ┤ ņל ņĪ░ņĀłļÉśļŖö ĒÖśņ×ÉņŚÉņä£ļŖö ļ░£ņāØĒĢśņ¦Ć ņĢŖĻĖ░ ļĢīļ¼ĖņŚÉ Quantitative Myasthenia Gravis (QMG) ņĀÉņłśĻ░Ć 8ņĀÉ ļ»Ėļ¦īņØ┤Ļ▒░ļéś ĒÅÉĒÖ£ļ¤ēņØ┤ ņśłņĖĪĒÅÉĒÖ£ļ¤ēņØś 70% ņØ┤ņāüņØ╝ ļĢīļŖö ņłśņłĀ ņĀä ņśłļ░®ņ╣śļŻīĻ░Ć ĒĢäņÜöĒĢśņ¦Ć ņĢŖļŗż[19].
ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Øņ£äĻĖ░ļŖö ņéĮĻ┤ĆĻ│╝ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░Ļ╣īņ¦Ć ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖĻ│Ā BiPAPņ£╝ļĪ£ ņ╣śļŻīĻ░Ć Ļ░ĆļŖźĒĢ£ Ļ▓ĮņÜ░Ļ░Ć ļ¦Äņ¦Ćļ¦ī, ņŗ¼ĒĢ£ ņł©ļćīļ¦łļ╣ä, ņŗ¼ĒĢ£ Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØ┤ļéś ņĀĆņé░ņåīĒśłņ”Ø, BiPAPņŚÉ ĻĖłĻĖ░ņØĖ ĒÖśņ×ÉļŖö ņéĮĻ┤ĆĻ│╝ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢ£ļŗż. ĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ļ¢╝ļŖö ņŗ£ļÅäļŖö ņĢäņ╣©ņŚÉ ņŗ£Ē¢ēĒĢśĻ│Ā, ņżæņ”ØĻĘ╝ļ¼┤ļĀźņ”Øņ£äĻĖ░ ĒÖśņ×ÉņØś ņĢĮ 20-40% ĒÖśņ×ÉĻ░Ć Ļ┤ĆņØä ņĀ£Ļ▒░ĒĢśļŖö ļŹ░ņŚÉ ņŗżĒī©ĒĢśņŚ¼ ņ×¼ņéĮĻ┤ĆņØ┤ ĒĢäņÜöĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņżæĒÖśņ×ÉņŗżņŚÉņä£ 48ņŗ£Ļ░ä ļÅÖņĢł Ļ░Éņŗ£ĒĢ┤ņĢ╝ ĒĢ£ļŗż. BiPAPņØ┤ļéś Ļ│Āņ£Āļ¤ēņĮöņéĮņ×ģĻ┤Ć(high-flow nasal cannula)ņØä ņé¼ņÜ®ĒĢśņŚ¼ Ļ┤Ć ņĀ£Ļ▒░ Ēøä ņ×¼ņéĮĻ┤ĆņØś ĒÖĢļźĀņØä ņżäņØ╝ ņłś ņ׳ļŗż[5,9,19].
ĻĘ╝ņ£äņČĢņĖĪņéŁĻ▓ĮĒÖöņ”Øņ£╝ļĪ£ ņØĖĒĢ£ Ļ░Ćņן ĒØöĒĢ£ ņé¼ļ¦ØņøÉņØĖņØĆ ĒśĖĒØĪļČĆņĀäņØ┤ļŗż. ļ╣äņ╣©ņŖĄĒÖśĻĖ░ņÖĆ ņ╣©ņŖĄĒÖśĻĖ░ ļ¬©ļæÉ ĻĘ╝ņ£äņČĢņĖĪņéŁĻ▓ĮĒÖöņ”ØņØś ĒśĖĒØĪļČĆņĀä ņ╣śļŻīņŚÉ ņżæņÜöĒĢ£ ņŚŁĒĢĀņØä ĒĢśĻ│Ā ņāØņĪ┤ņØä ņŚ░ņןĒĢ£ļŗż.
American College of Chest PhysiciansņŚÉ ņØśĒĢ£ ņ×äņāüņ¦äļŻīņ¦Ćņ╣©ņŚÉ ļö░ļź┤ļ®┤ ĻĘ╝ņ£äņČĢņĖĪņéŁĻ▓ĮĒÖöņ”ØņØä ĒżĒĢ©ĒĢ┤ņä£ ļ¦īņä▒ĒśĖĒØĪļČĆņĀäņØä ņ£Āļ░£ĒĢśļŖö ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉļŖö 6Ļ░£ņøö ļ¦łļŗż ĒÅÉĻĖ░ļŖźĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśĻ│Ā ĒśĖĒØĪļČĆņĀä ņ”ØņāüņØ┤ ņ׳ļŖöņ¦Ć ĒÖĢņØĖĒĢ┤ņĢ╝ ĒĢ£ļŗż. ĒśĖĒØĪļČĆņĀä ņ”ØņāüņØ┤ ņ׳Ļ│Ā Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ēņØ┤ ņśłņĖĪĻ░ÆņØś 80% ļ»Ėļ¦īņØ┤Ļ▒░ļéś, ņ”ØņāüņØ┤ ņŚåļŹöļØ╝ļÅä Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ēņØ┤ ņśłņĖĪĻ░ÆņØś 50% ļ»Ėļ¦īņØ╝ ļĢī, ņĄ£ļīĆ ļōżņł©ņĢĢņØ┤ 60 cmH2O ļ»Ėļ¦īņØ┤Ļ▒░ļéś ņĄ£ļīĆļéĀņł©ņĢĢņØ┤ 40 cmH2O ļ»Ėļ¦īņØ╝ ļĢī, ņĄ£ļīĆĻĖ░ņ╣©ņ£Āļ¤ēņØ┤ 270 L/min ļ»Ėļ¦īņØ╝ ļĢī, SNIPņØ┤ ļé©ņ×ÉļŖö 70 cmH2O ļ»Ėļ¦ī, ņŚ¼ņ×ÉļŖö 60 cmH2O ļ»Ėļ¦īņØ╝ ļĢī ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļź╝ ņŗ£ņ×æĒĢśļÅäļĪØ ĻČīĻ│ĀĒĢ£ļŗż. ĒÅÉĻĖ░ļŖźĻ▓Ćņé¼Ļ░Ć ņĀĢņāüņØ┤ļŹöļØ╝ļÅä ĒśĖĒØĪļČĆņĀä ņ”ØņāüņØ┤ ņ׳ļŗżļ®┤ ņĢ╝Ļ░äņé░ņåīĒżĒÖöļÅäņĖĪņĀĢņŚÉņä£ ņłśļ®┤ņŗ£Ļ░ä 2% ņØ┤ņāüņŚÉņä£ ņé░ņåīĒżĒÖöļÅäĻ░Ć 90% ņØ┤ĒĢśĻ▒░ļéś ļÅÖļ¦źĒśłĻĖ░ņ▓┤ņŚÉņä£ PaCO2Ļ░Ć 45 mmHg ņ┤łĻ│╝ņØ╝ ļĢīļÅä ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļź╝ ņŗ£ņ×æĒĢśļÅäļĪØ ĒĢ£ļŗż. ĻĘĖļ”¼Ļ│Ā ņĢ╝Ļ░äņé░ņåīĒżĒÖöļÅäņĖĪņĀĢĻ│╝ PaCO2ļÅä ņĀĢņāüņØ┤ņ¦Ćļ¦ī ĒśĖĒØĪļČĆņĀä ņ”ØņāüņØ┤ ņ׳ļŗżļ®┤ ņłśļ®┤ļŗżņøÉĻ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ļ¼┤ĒśĖĒØĪ-ņĀĆĒśĖĒØĪņ¦Ćņłś(apnea-hypopnea index)Ļ░Ć ņŗ£Ļ░äļŗ╣ 5ĒÜī ņØ┤ņāüņØ┤Ļ▒░ļéś 5ļČä ņØ┤ņāü ņé░ņåīĒżĒÖöļÅäĻ░Ć 88% ņØ┤ĒĢśņØ╝ ļĢīļŖö ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļź╝ ņŗ£ņ×æĒĢśļÅäļĪØ ĻČīĻ│ĀĒĢ£ļŗż[16]. ļ╣äņ╣©ņŖĄĒÖśĻĖ░ ņżæņŚÉ ņł©ļćīļ¦łļ╣äĻ░Ć ņŗ¼ĒĢ┤ņ¦ĆĻ▒░ļéś, ĒØĪņØĖņØ┤ ņ×ÉņŻ╝ ņØ╝ņ¢┤ļéśĻ▒░ļéś, ĻĖ░ņ╣©ņØä ņל ĒĢśņ¦Ć ļ¬╗ĒĢśĻ▒░ļéś, ĒÅÉļĀ┤ņØ┤ ļ░śļ│ĄļÉśĻ▒░ļéś, ĒÅÉĻĖ░ļŖźņØ┤ Ļ│äņåŹ ņĀĆĒĢśļÉśĻ│Ā ĒÖśņ×ÉĻ░Ć ĻĖ░Ļ┤ĆņĀłĻ░£ļź╝ ņøÉĒĢ£ļŗżļ®┤ ĻĖ░Ļ┤ĆņĀłĻ░£ņÖĆ ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ņŗ£Ē¢ēĒĢ£ļŗż[16].
ņé╝Ēé┤Ļ│żļ×ĆņØĆ ĒØĪņØĖ ņ£äĒŚśņØä ņ”ØĻ░Ćņŗ£ĒéżĻ│Ā, ņ▓┤ņżæĻ░ÉņåīņÖĆ ņśüņ¢æņŗżņĪ░ļź╝ ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŗż. Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ēņØ┤ ņśłņĖĪĻ░ÆņØś 50% ļ»Ėļ¦īņØ┤ļ®┤ Ēö╝ļČĆĻ▓Įņ£Āļé┤ņŗ£Ļ▓Įņ£äņ░ĮļāäņłĀ(percutaneous endoscopic gastrostomy) ņØ┤ļéś ļ░®ņé¼ņäĀņéĮņ×ģņ£äņ░ĮļāäņłĀ(radiologically inserted gastrostomy) ņŗ£ņłĀņŚÉ ļö░ļźĖ ņ£äĒŚśņØ┤ ņ”ØĻ░ĆĒĢśļ»ĆļĪ£ Ļ░ĢņĀ£ĒÅÉĒÖ£ļ¤ēņØ┤ ņśłņĖĪĻ░ÆņØś 50% ļ»Ėļ¦īņØ┤ ļÉśĻĖ░ ņĀäņŚÉ ņŗ£Ē¢ēĒĢśļŖö Ļ▓āņØ┤ ĻČīņןļÉ£ļŗż[5,20].
ĻĖēņä▒ĒśĖĒØĪļČĆņĀäņØĆ ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņŚÉņä£ Ļ░Ćņן ņŗ¼Ļ░üĒĢ£ ĒĢ®ļ│æņ”ØņØ┤ļŗż. ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņŚÉņä£ ļéśĒāĆļéśļŖö ĒśĖĒØĪļČĆņĀäņØä ņØ┤ĒĢ┤ĒĢśĻ│Ā ĒÖśņ×ÉņØś ņ×äņāüņåīĻ▓¼, ĒÅÉĻĖ░ļŖźĻ▓Ćņé¼, SpO2, PaCO2 ļō▒ ņŚ¼ļ¤¼ ņ¦ĆĒæ£ļōżņØä ĒåĄĒĢ┤ ĒśĖĒØĪļČĆņĀäņØä ņśłņĖĪĒĢśņŚ¼ ņĀüņĀłĒĢ£ ņŗ£ĻĖ░ņŚÉ ņ╣śļŻīĒĢśņŚ¼ ĒĢ®ļ│æņ”ØĻ│╝ ņé¼ļ¦ØņØä ņżäņØ╝ ņłś ņ׳ļŗż. ĒśĖĒØĪņ”ØņāüņØĆ ĒśĖĒØĪĻĘ╝ņ£ĪņØ┤ ņŗ¼ĒĢśĻ▓ī ņĢĮĒĢ┤ņ¦ä Ēøä ļéśĒāĆļéĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ĒÅÉĻĖ░ļŖźņØä ņĀĢĻĖ░ņĀüņ£╝ļĪ£ ĒÅēĻ░ĆĒĢśĻ│Ā Ļ░Éņŗ£ĒĢśļŖö Ļ▓āņØ┤ ĒĢäņÜöĒĢśļŗż. ĒÖśĻĖ░ņןņĢĀĻ░Ć ņ׳ļŖö ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖś ĒÖśņ×ÉņØś ĒśĖĒØĪļČĆņĀäņŚÉņä£ ņé░ņåīņÜöļ▓ĢņØĆ ņśżĒ׳ļĀż Ļ│ĀņØ┤ņé░ĒÖöĒāäņåīĒśłņ”ØņØä ņĢģĒÖöņŗ£Ēé¼ ņłś ņ׳Ļ│Ā, ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļéś ņ╣©ņŖĄĻĖ░Ļ│äĒÖśĻĖ░ļź╝ ĒåĄĒĢ┤ ĒÖśĻĖ░ļ│┤ņĪ░ļź╝ ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢ£ļŗż. ņŗ¼ĒĢ£ ņł©ļćīļ¦łļ╣äĻ░Ć ņŚåļŗżļ®┤ ļ╣äņ╣©ņŖĄĒÖśĻĖ░ļź╝ Ļ│ĀļĀżĒĢśĻ│Ā ĻĖ░ņ╣©ņØä ņ£ĀļÅäĒĢśļŖö ļ░®ļ▓ĢļōżļÅä ļ│æĒ¢ēĒĢśļŖö Ļ▓āņØ┤ ļÅäņøĆņØ┤ ļÉ£ļŗż.
ĻĖēņä▒ ņŗĀĻ▓ĮĻĘ╝ņ£ĪĒśĖĒØĪļČĆņĀäņØĆ ņŗĀĻ▓ĮĻ│╝ ņØśņé¼ņŚÉĻ▓ī ņ¢┤ļĀżņÜ┤ Ļ│╝ņĀ£ņ¦Ćļ¦ī ĒśĖĒØĪļČĆņĀäņØä ņØ┤ĒĢ┤ĒĢśĻ│Ā ņĀüņĀłĒĢ£ ņŗ£ĻĖ░ņŚÉ ņĀüņĀłĒĢ£ ļ░®ļ▓Ģņ£╝ļĪ£ ņ╣śļŻīĒĢśņŚ¼ ĒÖśņ×ÉņØś ņāØņĪ┤Ļ│╝ ņéČņØś ņ¦łņØä Ē¢źņāüņŗ£Ēé¼ ņłś ņ׳ĻĖ░ļź╝ ĻĖ░ļīĆĒĢ£ļŗż.
Table┬Ā1.
Risk of respiratory insufficiency within seven days in patients with Guillain-Barre syndrome using Erasmus GBS Respiratory Insufficiency scores
| Feature | EGRISa | |
|---|---|---|
| Medical research Counsil sum score | 51-60 | 0 |
| 41-50 | 1 | |
| 31-40 | 2 | |
| 21-30 | 3 | |
| Ōēż20 | 4 | |
| Days between weakness onset and hospital admission | >7 | 0 |
| 4-7 | 1 | |
| <4 | 2 | |
| Facial or bulbar weakness | Absent | 0 |
| Present | 1 |
REFERENCES
2. Choi YJ, Cho JH. Current status of treatment of acute respiratory failure in Korea. J Korean Med Assoc 2022;65:124-129.

4. Pfeffer G, Povitz M. Respiratory management of patients with neuromuscular disease: current perspectives. Degener Neurol Neuromuscul Dis 2016;6:111-118.



6. Rabinstein AA. Acute neuromuscular respiratory failure. CONTIN Lifelong Learn Neurol 2015;21:1324-1345.

8. Chen TH, Hsu JH. Noninvasive ventilation and mechanical insufflator-exsufflator for acute respiratory failure in children with neuromuscular disorders. Front Pediatr 2020;8:593282.



9. Rezania K, Goldenberg FD, White S. Neuromuscular disorders and acute respiratory failure: diagnosis and management. Neurol Clin 2012 30:161-185. viii.


11. Choi WA. Pulmonary rehabilitation of restrictive lung diseases. Ann Cardiopulm Rehabil 2021;1:33-41.

13. Yoo I, Choi SJ, Sung JJ. Application of respiratory function tests in patients with neurological diseases. Ann Clin Neurophysiol 2023;25:1-9.

14. Murray NM, Reimer RJ, Cao M. Acute on chronic neuromuscular respiratory failure in the intensive care unit: optimization of triage, ventilation modes, and extubation. Cureus 2021;13:e16297.



15. Shang P, Feng J, Wu W, Zhang HL. Intensive care and treatment of severe Guillain-Barr├® syndrome. Front Pharmacol 2021;12:608130.



16. Khan A, Frazer-Green L, Amin R, Wolfe L, Faulkner G, Casey K, et al. Respiratory management of patients with neuromuscular weakness: an American College of Chest Physicians clinical practice guideline and expert panel report. Chest 2023 Mar 13 [Epub]. DOI: 10.1016/j.chest.2023.03.011.
17. Bureau C, Demoule A. Weaning from mechanical ventilation in neurocritical care. Rev Neurol (Paris) 2022;178:111-120.


-
METRICS

-
- 0 Crossref
- Scopus
- 756 View
- 19 Download
- Related articles in Korean J Neuromuscul Disord
-
Autoantibody Testing in Neuromuscular Disorders2022 June;14(1)