ĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ļŖö Ēīöļŗżļ”¼ņØś ĻĘ╝ļĀź ņĢĮĒÖöļź╝ ĒŖ╣ņ¦Ģņ£╝ļĪ£ ĒĢśļŖö ņ×äņāüņĀü ļ░Å ņ£ĀņĀäņĀüņ£╝ļĪ£ļÅä ļŗżņ¢æĒĢ£ ņ£ĀņĀäņä▒ ņŗĀĻ▓ĮĻĘ╝ņ£Īņ¦łĒÖśņØ┤ļŗż. ĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ņØś ņøÉņØĖņ£ĀņĀäņ×ÉļĪ£ Ēśäņ×¼Ļ╣īņ¦Ć 62Ļ░£ņØś ņ£ĀņĀäņ×ÉĻ░Ć ĻĘ£ļ¬ģļÉśņ¢┤ ņ׳ļŗż[1]. ņØ┤ ņżæ CAV3 ņ£ĀņĀäņ×ÉņØś ļ│æņøÉņä▒ ļ│ĆņØ┤ņŚÉ ņØśĒĢ┤ ņ£Āļ░£ļÉśļŖö ņ╣┤ļ▓Āņś¼ļ”░ļ│æ(caveolinopathy)ņØĆ ņä£ņä£Ē׳ ņ¦äĒ¢ēĒĢśļŖö ļ¬Ėņ¬Į ĻĘ╝ņ£ĪņØś ņĢĮĒÖöņÖĆ Ēśłņżæ Ēü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£(creatine kinase)ņØś ņāüņŖ╣, ĻĘ╝ņ£ĪņäĖĒżņØś Ļ┤┤ņé¼ ļ░Å ņ×¼ņāØņØä ĒŖ╣ņ¦Ģņ£╝ļĪ£ ĒĢśļŖö Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝(limb-girdle muscular dystrophy)ļź╝ ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŗż[2]. ĻĘĖļ¤¼ļéś CAV3 ņ£ĀņĀäņ×ÉņØś ļ│æņøÉņä▒ ļ│ĆņØ┤ņØś ņ×äņāüĒæ£ĒśäĒśĢņØĆ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ ņÖĖņŚÉļÅä ņ×öļ¼╝Ļ▓░ĻĘ╝ņ£Īļ│æ(rippling muscle disease), Ļ│ĀĒü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£Ēśłņ”Ø, ļ©╝ņ¬Į ĻĘ╝ņ£Īļ│æ(distal myopathy) ļō▒ņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳ņ£╝ļ®░ ļŗżņ¢æĒĢ£ Ēæ£ĒśäĒśĢ Ļ░äņØś ņ×äņāüņĀü Ļ▓╣ņ╣©ņØ┤ ņ׳ļŗż[3]. ņŗ¼ņ¦Ćņ¢┤ CAV3 ņ£ĀņĀäņ×ÉņØś ļÅÖņØ╝ĒĢ£ ļ│æņøÉņä▒ ļ│ĆņØ┤ļź╝ Ļ░¢Ļ│Ā ņ׳ļŖö ĒĢ£ Ļ░ĆņĪ▒ ļé┤ņŚÉņä£ļÅä ĒÖśņ×ÉļōżņØś Ēæ£ĒśäĒśĢņØ┤ ņä£ļĪ£ ļŗżļźĖ Ļ▓āņØ┤ ļ│┤Ļ│ĀļÉśĻĖ░ļÅä ĒĢśņśĆļŗż.4 ņØ┤ļ¤¼ĒĢ£ ņ×äņāüņĀü ļŗżņ¢æņä▒ņØĆ ņ╣┤ļ▓Āņś¼ļ”░ļ│æņØś ņ¦äļŗ©ņØä ņ¢┤ļĀĄĻ▓ī ļ¦īļōĀļŗż. ņĀĆņ×ÉļōżņØĆ CAV3 ņ£ĀņĀäņ×ÉņØś ļ│æņøÉņä▒ ļ│ĆņØ┤ļź╝ Ļ░¢ļŖö ĒĢ£ĻĄŁņØĖ ĒĢ£ Ļ░ĆņĪ▒ņŚÉņä£ ĒĢ£ ļ¬ģņØĆ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ļź╝, ļŗżļźĖ ļæÉ ļ¬ģņØĆ Ļ│ĀĒü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£Ēśłņ”ØņØä Ļ░¢ļŖö Ļ░ĆņĪ▒ ļé┤ ņ×äņāüņĀü ļŗżņ¢æņä▒ņØä ĒÖĢņØĖĒĢśņśĆĻĖ░ņŚÉ ņØ┤ļź╝ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņ”Ø ļĪĆ
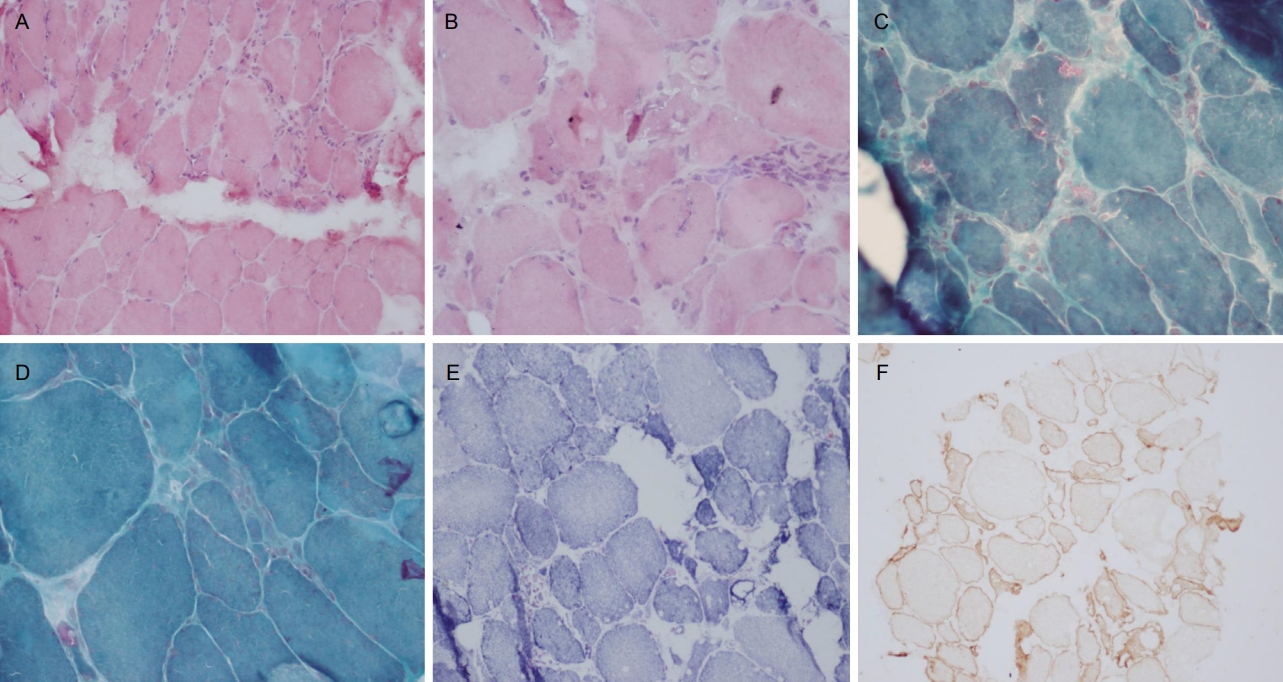
32ņäĖ ļé©ņ×É ĒÖśņ×É(Fig. 1A, III-1)Ļ░Ć ņä£ņä£Ē׳ ņ¦äĒ¢ēĒĢśļŖö ņ¢æ Ēīöļŗżļ”¼ņØś ĻĘ╝ļĀź ņĀĆĒĢśļĪ£ ļ░®ļ¼ĖĒĢśņśĆļŗż. 10ņäĖ ņ┤łļ░śļČĆĒä░ Ēīöļŗżļ”¼ņØś ĻĘ╝ļĀźņØ┤ ņĢĮĒ¢łĻ│Ā ĒīöĻĄĮĒśĆĒÄ┤ĻĖ░ļź╝ ņĀäĒśĆ ļ¬╗Ē¢łļŗżĻ│Ā ĒĢśņśĆļŗż. 32ņäĖļČĆĒä░ Ļ│äļŗ© ņśżļź╝ ļĢī ņ×ÉņŻ╝ ļäśņ¢┤ņĀĖņä£ ļ│æņøÉņØä ļ░®ļ¼ĖĒĢśņśĆļŗż. ĒÖśņ×ÉļŖö Ļ░äĒŚÉņĀüņØĖ ĻĘ╝ņ£ĪĒåĄņØä ĒśĖņåīĒĢśņśĆņ£╝ļéś ņŗ¼ĒĢśņ¦ĆļŖö ņĢŖņĢśļŗż. 32ņäĖņŚÉ ņŗ£Ē¢ēĒĢ£ ņŗĀĻ▓ĮĒĢÖņĀü ņ¦äņ░░ņŚÉņä£ ņ¢æ ņóģņĢäļ”¼ ĻĘ╝ņ£ĪņØś Ļ░Ćņä▒ ļ╣äļīĆ ņåīĻ▓¼Ļ│╝ Ēīöļŗżļ”¼ņØś ļ¬Ėņ¬Į ĻĘ╝ņ£ĪņØś ĻĘ╝ļĀź ņĢĮĒÖöļź╝ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. Medical Research CouncilņØä ņØ┤ņÜ®ĒĢ£ ĻĘ╝ļĀźĻ▓Ćņé¼ņŚÉņä£ ņ¢æņ¬Į ņāüņ¦Ć ļ¬Ėņ¬Į ĻĘ╝ņ£ĪņØĆ 4ļō▒ĻĖē, ņĢäļלĒīö ĻĘ╝ņ£ĪĻ│╝ ņłśļČĆ ĻĘ╝ļĀźņØĆ 5ļō▒ĻĖēņØ┤ņŚłļŗż. ņ¢æņĖĪ ĒĢśņ¦Ć ļ¬Ėņ¬Į ĻĘ╝ņ£ĪņØĆ 4ļō▒ĻĖē, ļ©╝ņ¬Į ĻĘ╝ņ£ĪņØĆ 5ļō▒ĻĖēņØ┤ņŚłļŗż. ĒÖśņ×ÉļŖö ļÅģļ”Į ļ│┤Ē¢ēņØ┤ Ļ░ĆļŖźĒĢśņśĆļŗż. Ļ░ÉĻ░ü Ļ▓Ćņé¼ļŖö ļ¬©ļæÉ ņĀĢņāüņØ┤ņŚłļŗż. ĒśłņĢĪ Ēü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£ļŖö 1,908 IU/L (ņ░ĖĻ│Āņ╣ś: 55-170 IU/L)ļĪ£ ņ”ØĻ░ĆļÉśņŚłļŗż. ņ╣©ĻĘ╝ņĀäļÅäĻ▓Ćņé¼ņŚÉņä£ ĻĘ╝ņ£Īļ│æņŚÉ ĒĢ®ļŗ╣ĒĢ£ ņåīĻ▓¼ņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż. ņóīņĖĪ ņ£äĒīöļæÉĻ░łļלĻĘ╝(biceps brachii)ĻĘ╝ņ£ĪņŚÉņä£ ĻĘ╝ņ£ĪņĪ░ņ¦üĻ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż(Fig. 2). ĻĘ╝ņ£ĪņĪ░ņ¦üĻ▓Ćņé¼ņŚÉņä£ ĻĘ╝ņä¼ņ£Ā Ēü¼ĻĖ░ņØś ļŗżņ¢æņä▒ņØ┤ ĒśäņĀĆĒĢśĻ▓ī ņ”ØĻ░ĆļÉśņ¢┤ ņ׳ņŚłĻ│Ā, Ļ┤┤ņé¼ļÉ£ ĻĘ╝ņäĖĒżņÖĆ ņ×¼ņāØ ĻĘ╝ņäĖĒżĻ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż. ņ╣┤ļ▓Āņś¼ļ”░ 3ņŚÉ ļīĆĒĢ£ ļ®┤ņŚŁņĪ░ņ¦üĒÖöĒĢÖņŚ╝ņāēĻ▓Ćņé¼ļŖö ņĀĢņāüņĀüņØĖ ļŗ©ļ░▒ ļ░£ĒśäņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż. ĒÖśņ×ÉļŖö ņ×äņāü ņ¢æņāüĻ│╝ ĻĘ╝ņ£ĪņĪ░ņ¦üĻ▓Ćņé¼ļź╝ ļ░öĒāĢņ£╝ļĪ£ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ņ£╝ļĪ£ ņ¦äļŗ©ļÉśņŚłļŗż. ĻĘ╝ļĀź ņĢĮĒÖöļŖö ņä£ņä£Ē׳ ņ¦äĒ¢ēĒĢ┤ņä£ 39ņäĖņŚÉ ĒÖśņ×ÉļŖö ĒÅēņ¦ĆņŚÉņä£ ļÅģļ”Įļ│┤Ē¢ēņØĆ Ļ░ĆļŖźĒĢśņśĆņ£╝ļéś ļ░öļŗźņŚÉņä£ ņĢēņĢśļŗżĻ░Ć ņŖżņŖżļĪ£ ņØ╝ņ¢┤ļéĀ ņłśļŖö ņŚåņŚłļŗż. 39ņäĖņŚÉ ņĀäņןņŚæņå£ņŚ╝ĻĖ░ņä£ņŚ┤ļČäņäØ(whole exome sequencing)Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā CAV3 ņ£ĀņĀäņ×ÉņØś NM_033337.3: c.296A>C (p.His99Pro) ņØ┤ĒśĢņĀæĒĢ®ļ│ĆņØ┤ļź╝ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 1B).
Ļ░ĆņĪ▒ ĻĄ¼ņä▒ņøÉņŚÉ ļīĆĒĢ┤ņä£ Ļ│ĀņĀäņĀü ņŚ╝ĻĖ░ņä£ņŚ┤ļČäņäØ(Sanger sequencing) ņØä ņŗ£Ē¢ēĒĢśņŚ¼ ĒĢ┤ļŗ╣ ļ│ĆņØ┤ļź╝ ĒÖĢņØĖĒĢśņśĆļŗż. ņ¢┤ļ©Ėļŗł(Fig. 1A, II-5)ņÖĆ ļé©ļÅÖņāØ(Fig. 1A, III-2)ļÅä ĒĢ┤ļŗ╣ ļ│ĆņØ┤ļź╝ Ļ░¢Ļ│Ā ņ׳ņŚłļŗż. ņ¢┤ļ©ĖļŗłļŖö ĻĘ╝ļĀź ņĢĮĒÖöļź╝ ĒśĖņåīĒĢśņ¦Ć ņĢŖņĢśĻ│Ā ļé©ļÅÖņāØņØĆ Ēö╝ļĪ£Ļ░ÉņØä ĒśĖņåīĒĢśņśĆņ£╝ļéś ņŗĀĻ▓ĮĒĢÖņĀü ņ¦äņ░░ņŚÉņä£ ĻĘ╝ļĀź ņĢĮĒÖöļŖö ņŚåņŚłļŗż. ļæÉ ņé¼ļ×ī ļ¬©ļæÉ ņ╣©ĻĘ╝ņĀäļÅäĻ▓Ćņé¼ņŚÉņä£ ĻĘ╝ņ£Īļ│æņØä ņŗ£ņé¼ĒĢśļŖö ņåīĻ▓¼ņØĆ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśĻ│Ā ļæÉ ĒÖśņ×É(II-5ņÖĆ III-2)ņØś ĒśłņĢĪ Ēü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£ļŖö Ļ░üĻ░ü 317 IU/LņÖĆ 819 IU/LļĪ£ ņāüņŖ╣ļÉśņ¢┤ ņ׳ņŚłļŗż. ļ│æņøÉņä▒ ļ│ĆņØ┤ ĒÖĢņØĖ Ēøä ĒÖśņ×É(III-1)ņÖĆ ņ¢┤ļ©Ėļŗł(II-5)ņÖĆ ļé©ļÅÖņāØ(III-2)ņŚÉĻ▓īņä£ ļ¼╝ļ”¼ņĀü ņ×ÉĻĘ╣ņŚÉ ņØśĒĢ┤ ļ¼╝Ļ▓░ ļ¬©ņ¢æņØś ĻĘ╝ņ£Ī ņłśņČĢ ļ░Å ĻĘ╝ņ£Ī ņ£ĄĻĖ░Ļ░Ć ņ׳ļŖöņ¦Ćļź╝ ĒÖĢņØĖĒĢśņśĆņ£╝ļéś Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. ļö░ļØ╝ņä£, ĒÖśņ×ÉļŖö Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ļĪ£ ļæÉ Ļ░ĆņĪ▒(II-5ņÖĆ III-2)ņØĆ Ļ│ĀĒü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£Ēśłņ”Øņ£╝ļĪ£ ņ¦äļŗ©ĒĢśņśĆļŗż.
Ļ│Ā ņ░░
ļ│Ė ņ”ØļĪĆņŚÉņä£ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ļź╝ Ļ░¢ļŖö ĒÖśņ×ÉņŚÉņä£ ņĀäņןņŚæņå£ņŚ╝ĻĖ░ņä£ņŚ┤ļČäņäØņØä ĒåĄĒĢ┤ CAV3 ņ£ĀņĀäņ×ÉņØś ļ│æņøÉņä▒ ļ│ĆņØ┤ļź╝ ĻĘ£ļ¬ģĒĢ£ Ēøä Ļ│ĀĒü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£Ēśłņ”Øļ¦ī ņ׳ļŖö ļŗżļźĖ Ļ░ĆņĪ▒ņŚÉņä£ļÅä ĒĢ┤ļŗ╣ ļ│ĆņØ┤ļź╝ ĒÖĢņØĖĒĢśņśĆļŗż. ņØ┤ ļ│ĆņØ┤Ļ░Ć ņ׳ļŖö ĒÖśņ×ÉņŚÉņä£ ļ¬©ļæÉ Ļ░ÖņØĆ ņ×äņāüĒæ£ĒśäĒśĢņØ┤ ņ׳ļŖö Ļ▓āņØĆ ņĢäļŗłņŚłņ£╝ļéś ļŗżņØīņØś ņØ┤ņ£ĀļĪ£ ĒĢ┤ļŗ╣ ņ£ĀņĀäņ×ÉĻ░Ć ņØ┤ Ļ░ĆņĪ▒ņŚÉņä£ ļ│┤ņØ┤ļŖö ĻĘ╝ņ£Īļ│æņØś ņ£ĀņĀäĒĢÖņĀü ņøÉņØĖņ£╝ļĪ£ ĒīÉļŗ©ĒĢśņśĆļŗż. 1) ĒĢ┤ļŗ╣ ļ│ĆņØ┤Ļ░Ć ņ׳ļŖö ņ£äņ╣śņŚÉ ļ│æņøÉņä▒ ļÅīņŚ░ļ│ĆņØ┤Ļ░Ć ļ¦ÄņØ┤ ļ│┤Ļ│ĀļÉśļŖö ņ£äņ╣śņØ┤ļŗż. 2) ĒĢ┤ļŗ╣ ļ│ĆņØ┤ļŖö ļŗżļźĖ ņĀĢņāüņØĖņØś ļŹ░ņØ┤Ēä░ļ▓ĀņØ┤ņŖżņŚÉņä£ļŖö ļ│┤Ļ│ĀĻ░Ć ļÉśņ¦Ć ņĢŖņØĆ ļ│ĆņØ┤ņØ┤ļŗż. 3) ĒĢ┤ļŗ╣ ļ│ĆņØ┤ļŖö ņŚ¼ļ¤¼ ņ╗┤Ēō©Ēä░ ĻĖ░ļ░śņØś ļČäņäØņŚÉņä£ ĒĢ┤ļŗ╣ ņ£ĀņĀäņ×É ļśÉļŖö ļŗ©ļ░▒ņ¦łņŚÉ ņ╣śļ¬ģņĀüņØĖ ĒÜ©Ļ│╝ļź╝ ņ£Āļ░£ĒĢĀ Ļ▓āņ£╝ļĪ£ ņśłņāüļÉśņŚłļŗż. 4) ĒĢ┤ļŗ╣ ļ│ĆņØ┤ļŖö ņĄ£ĻĘ╝ ņŚ░ĻĄ¼ņŚÉņä£ ļ│æņøÉņä▒ ļ│ĆņØ┤ļĪ£ ļ│┤Ļ│ĀļÉ£ ņĀüņØ┤ ņ׳ņŚłļŗż[5]. ļö░ļØ╝ņä£ ļ»ĖĻĄŁņØśĒĢÖņ£ĀņĀäĒĢÖĒÜīņØś ĻĖ░ņżĆņŚÉ ļö░ļØ╝ņä£ ĒĢ┤ļŗ╣ ļ│ĆņØ┤ļŖö ļ│æņøÉņä▒ ļ│ĆņØ┤ļĪ£ ņ¦äļŗ©ĒĢĀ ņłś ņ׳ņŚłļŗż[6].
ņ╣┤ļ▓Āņś¼ļ”░(caveolin)ņØĆ ņäĖĒżļ¦ēņØś ņ╣┤ļ▓Āņś¼ļØ╝(caveolae)ļź╝ ĻĄ¼ņä▒ĒĢśļŖö ņŻ╝ļÉ£ ļŗ©ļ░▒ņ¦łļĪ£ņä£ ņäĖĒżļé┤ ņŗĀĒśĖ ņĀäļŗ¼, ņåīĒż ņłśņåĪņØä ļŗ┤ļŗ╣ĒĢśļ®░ ņ╣┤ļ▓Āņś¼ļ”░1, 2, 3ņØś ņäĖ ņóģļźśĻ░Ć ņĢīļĀżņĀĖ ņ׳ļŗż. ĻĘĖņżæ CAV3 ņ£ĀņĀäņ×ÉņŚÉ ņØśĒĢ┤ņä£ ļ░£ĒśäļÉśļŖö ņ╣┤ļ▓Āņś¼ļ”░3 (caveolin-3)ņØĆ ĻĘ╝ņ£ĪņäĖĒżņŚÉņä£ļ¦ī ĒŖ╣ņØ┤ņĀüņ£╝ļĪ£ ļ░£ĒśäĒĢśĻ│Ā ļööņŖżĒŖĖļĪ£ĒĢĆ ļŗ╣ļŗ©ļ░▒ņ¦ł ļ│ĄĒĢ®ņ▓┤ņŚÉ ņŚ░Ļ┤ĆļÉśņ¢┤ ĻĘ╝ņ£Ī ņäĖĒżļ¦ē ņĢłņĀĢņä▒ņØä ņ£Āņ¦ĆĒĢśļŖö ņŚŁĒĢĀņØä ĒĢ£ļŗż[7]. CAV3 ļŗ©ļ░▒ņ¦łņØĆ C-ļ¦Éļŗ©, N-ļ¦Éļŗ©, ņżæĻ░ä ņåīņłśņä▒ ļČĆļČäņ£╝ļĪ£ ņØ┤ļŻ©ņ¢┤ņĀĖ ņ׳ļŗż. ĒŖ╣Ē׳ ņØ┤ ņżæĻ░ä ņåīņłśņä▒ ļČĆļČäņØĆ ņäĖĒżļ¦ēņŚÉ ņ£äņ╣śĒĢśļŖö ļČĆļČäņØ┤ļ®░, ņ╣┤ļ▓Āņś¼ļ”░ ļŗ©ļ░▒ņ¦ł ņś¼ļ”¼Ļ│Āļ©Ė ļ░Å ņ╣┤ļ▓Āņś¼ļØ╝ ĒśĢņä▒ņŚÉ ĒĢäņłśņĀüņØĖ ļČĆļČäņØ┤ļŗż. ņØ┤ļ¤¼ĒĢ£ ņØ┤ņ£ĀļĪ£ ņżæĻ░ä ņåīņłśņä▒ ņśüņŚŁņŚÉņä£ ļ░£ņāØĒĢ£ CAV3 ļ│æņĀü ļ│ĆņØ┤ļŖö Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ņÖĆ Ļ░ÖņØĆ ņŗ¼ĒĢ£ Ēæ£ĒśäĒśĢņØä ļéśĒāĆļé┤Ļ│Ā, ļéśļ©Ėņ¦Ć ņśüņŚŁņŚÉņä£ ļ░£ņāØĒĢĀ Ļ▓ĮņÜ░ ņ×äņāüņĀüņ£╝ļĪ£ ņĢĮĒĢ£ Ēæ£ĒśäĒśĢņØä ļ│┤ņØ╝ Ļ▓āņØ┤ļØ╝ļŖö Ļ░ĆņäżļÅä ņĀ£ĻĖ░ļÉśņŚłļŗż[7,8]. ļ│Ė ņ”ØļĪĆņŚÉņä£ ĒÖĢņØĖļÉ£ ņØ┤ĒśĢ ņĀæĒĢ® Ļ│╝ņśżļÅīņŚ░ļ│ĆņØ┤ņØĖ c.296A>C (p.His99Pro)ļŖö 2020ļģäņŚÉ ĒĢ£ ņ░©ļĪĆ ļ│┤Ļ│ĀļÉśņŚłļŹś ļ│ĆņØ┤ļĪ£[5], ņØ┤ ļ│ĆņØ┤Ļ░Ć ļ░£ņāØĒĢ£ ņ£äņ╣śļŖö ņżæĻ░ä ņåīņłśņä▒ ņśüņŚŁņŚÉ ņåŹĒĢ£ļŗż. ĒĢśņ¦Ćļ¦ī ļ│Ė ņ”ØļĪĆļŖö ņżæĻ░ä ņåīņłśņä▒ ņśüņŚŁņŚÉņä£ ļ░£ņāØĒĢ£ Ļ░ÖņØĆ ļ│ĆņØ┤Ļ░Ć Ļ░ĆņĪ▒ ļé┤ņŚÉņä£ ņä£ļĪ£ ļŗżļźĖ ņĀĢļÅäņØś Ēæ£ĒśäĒśĢņØä ļ│┤ņØ┤ļŖö ņśłņŗ£ļź╝ ņ×ģņ”ØĒĢśņśĆļŗż. ļö░ļØ╝ņä£ ņ£ĀņĀäņ×É ļ│ĆņØ┤ņØś ņ£äņ╣śļ¦īņ£╝ļĪ£ļŖö ļŗżņ¢æĒĢ£ ņ×äņāü ņ”ØņāüņØä ņäżļ¬ģĒĢśļŖö ļŹ░ ĒĢ£Ļ│äĻ░Ć ņ׳ņ£╝ļ®░ ņØ┤ļ¤¼ĒĢ£ ņŚ░Ļ┤ĆĻ┤ĆĻ│äļź╝ ņ×ģņ”ØĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ļŹöņÜ▒ ļ¦ÄņØĆ ņé¼ļĪĆ ļ│┤Ļ│ĀņÖĆ ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢśļŗż.
ņØ┤ņÖĆ Ļ░ÖņØ┤ Ļ░ĆņĪ▒ ļé┤ņŚÉņä£ ĒĢśļéśņØś CAV3 ļ│æņĀü ļ│ĆņØ┤Ļ░Ć ļŗżņ¢æĒĢ£ Ēæ£ĒśäĒśĢņØä ļéśĒāĆļé┤ļŖö ņ”ØļĪĆļŖö ĻĖ░ņĪ┤ņŚÉļÅä ļ│┤Ļ│ĀļÉśņŚłļŗż. ĒĢ£ ļÅģņØ╝ Ļ░ĆĻ│äņŚÉņä£ ņŗ£Ē¢ēļÉ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļŗżņ¢æĒĢ£ Ļ░ĆņĪ▒ ļé┤ Ēæ£ĒśäĒśĢņØś ņ░©ņØ┤ļź╝ ļ│┤ņśĆļŗż. ņØ┤ ņŚ░ĻĄ¼ņŚÉņä£ ņŗĀĻ▓ĮĒĢÖņĀü ņ¦äņ░░ņØä ņŗ£Ē¢ēĒĢ£ 9ļ¬ģņØś ĒÖśņ×É ņżæņŚÉņä£ 2ļ¬ģņØĆ ņ×öļ¼╝Ļ▓░ĻĘ╝ņ£Īļ│æņØä ļÅÖļ░śĒĢ£ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ļĪ£ ņ¦äļŗ©ļÉśņŚłĻ│Ā 5ļ¬ģņØĆ ņ×öļ¼╝Ļ▓░ĻĘ╝ņ£Īļ│æņØä ļÅÖļ░śĒĢ£ ļ©╝ņ¬Į ĻĘ╝ņ£Īļ│æņ£╝ļĪ£ ņ¦äļŗ©ļÉśņŚłĻ│Ā 2ļ¬ģņØĆ ņ×öļ¼╝Ļ▓░ĻĘ╝ņ£Īļ│æļ¦ī ņ׳ļŗżĻ│Ā ņ¦äļŗ©ļÉśņŚłļŗż. ņØ┤ļ¤¼ĒĢ£ Ļ░ÖņØĆ ņ£ĀņĀäņ×ÉņŚÉņä£ņØś Ēæ£ĒśäĒśĢ ņ░©ņØ┤ļŖö ĒĢ┤ļŗ╣ ņ£ĀņĀäņ×É ņÖĖ ļŗżļźĖ ņ£ĀņĀäņ×ÉļōżņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢ£ļŗżĻ│Ā ņāØĻ░üļÉśņŚłļŗż[4].
ņĄ£ĻĘ╝ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ņŚÉ ļīĆĒĢ┤ ļ░£Ēæ£ļÉ£ ņāłļĪ£ņÜ┤ ļ¬ģļ¬ģļ▓Ģ ņ¦Ćņ╣©ņŚÉ ļö░ļź┤ļ®┤ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝1CļŖö Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ĻĄ░ņØ┤ ņĢäļŗī ņ×öļ¼╝Ļ▓░ĻĘ╝ņ£Īļ│æ2 (rippling muscle disease 2)ļĪ£ ņāłļĪŁĻ▓ī ļČäļźśļÉśņŚłļŗż[9]. CAV3 ņ£ĀņĀäņ×ÉņÖĆ ņŚ░Ļ┤ĆļÉ£ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ ĒÖśņ×ÉļōżņØ┤ ņ×öļ¼╝Ļ▓░ ĒśäņāüĻ│╝ ĻĘ╝ņ£ĪĒåĄņØä ņŻ╝ļĪ£ ĒśĖņåīĒĢśņśĆĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ļ│Ė ņ”ØļĪĆņŚÉņä£ III-1 ĒÖśņ×ÉļŖö ļ░öļĆÉ ļČäļźśļ▓ĢņŚÉ ļö░ļź┤ļ®┤ Ēæ£ĒśäĒśĢņØä ņ×öļ¼╝Ļ▓░ĻĘ╝ņ£Īļ│æ2ļĪ£ ļČäļźśĒĢśļŖö Ļ▓āņØ┤ ņĀüņĀłĒĢśļéś ņČöņĀüĻ▓Ćņé¼ņŚÉņä£ļÅä ņ×öļ¼╝Ļ▓░ ĒśäņāüņØä ĒÖĢņØĖĒĢśņ¦Ć ļ¬╗ĒĢśņśĆĻĖ░ņŚÉ ļ│ĖĻ│ĀņŚÉņä£ļŖö Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ļĪ£ Ēæ£ĒśäĒĢśņśĆļŗż.
Ēśäņ×¼Ļ╣īņ¦Ć ņ╣┤ļ▓Āņś¼ļ”░ļ│æņØś ļ│æļ”¼ĻĖ░ņĀäņØĆ ņĀĢĒÖĢĒ׳ ĻĘ£ļ¬ģļÉśņ¦Ć ņĢŖņĢśļŗż. ļŗżļ¦ī, CAV3 ņØ┤ĒśĢņĀæĒĢ®ļ│ĆņØ┤ņØś Ļ▓ĮņÜ░ļŖö ĻĖ░ņĪ┤ņØś ļ®┤ņŚŁņĪ░ņ¦ü ĒÖöĒĢÖ ļ░Å ņø©ņŖżĒä┤ ļĖöļĪ» ļČäņäØ Ļ▓░Ļ│╝ļź╝ ĒåĄĒĢ┤ ņÜ░ņä▒-ņØīņä▒ ĒÜ©Ļ│╝(dominant-negative effect)ņØś ĻĖ░ņĀäņ£╝ļĪ£ ņ×æņÜ®ĒĢĀ Ļ▓āņ£╝ļĪ£ ņČöņĖĪļÉśĻ│Ā ņ׳ļŗż[4,7]. ņØ┤ļź╝ ļÆĘļ░øņ╣©ĒĢĀ ņłś ņ׳ļŖö ņ”ØĻ▒░ļĪ£ ĻĄ¼ņĪ░ņØ┤ņāüņØś CAV3 ļŗ©ļ░▒ņ¦łņØ┤ ņĢ╝ņāØĒśĢ ļŗ©ļ░▒ņ¦łĻ│╝ ĒĢ©Ļ╗ś ļČłņĢłņĀĢĒĢ£ Ļ│ĀļČäņ×É ļŗ©ļ░▒ņ¦ł ņØæņ¦æņ▓┤ļź╝ ĒśĢņä▒ĒĢśņŚ¼ ļ╣Āļź┤Ļ▓ī ļČäĒĢ┤ļÉ£ļŗżļŖö ņŚ░ĻĄ¼ļÅä ņ׳ņŚłļŗż[10]. ņŗżņĀ£ļĪ£ ļ│Ė ņ”ØļĪĆņØś Ļ▓ĮņÜ░ļź╝ ļ│┤ļ®┤ ņ╣┤ļ▓Āņś¼ļ”░3ņŚÉ ļīĆĒĢ£ ļ®┤ņŚŁ ņĪ░ņ¦üĒÖöĒĢÖņŚ╝ņāēĻ▓Ćņé¼ņŚÉņä£ ņĀĢņāüņĀüņØĖ ļŗ©ļ░▒ ļ░£ĒśäņØ┤ ļ│┤ņśĆĻĖ░ ļĢīļ¼ĖņŚÉ ĻĖ░ļŖźņØś ņĀĆĒĢś ļĢīļ¼ĖņØ┤ļØ╝ĻĖ░ļ│┤ļŗżļŖö ņÜ░ņä▒-ņØīņä▒ĒÜ©Ļ│╝ņØś ļ│æļ”¼ĻĖ░ņĀäņØ┤ ņ×æņÜ®ĒĢśņśĆņØä Ļ▓āņ£╝ļĪ£ ņČöņĀĢĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ¤¼ļéś ņØ┤ņŚÉ ļīĆĒĢ┤ņä£ļŖö ņäĖĒż ļśÉļŖö ļÅÖļ¼╝ļ¬©ļŹĖņŚÉņä£ņØś ņČöĻ░ĆņĀüņØĖ ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢĀ Ļ▓āņØ┤ļŗż.
ņĀĆņ×ÉļōżņØĆ CAV3 ņ£ĀņĀäņ×ÉņØś ļ│æņøÉņä▒ ļ│ĆņØ┤ļź╝ Ļ░¢Ļ│Ā ņ׳ļŖö ĒĢ£ Ļ░ĆņĪ▒ņŚÉņä£ Ēīöļŗżļ”¼ņØ┤ņØīĻĘ╝ļööņŖżĒŖĖļĪ£Ēö╝ņÖĆ Ļ│ĀĒü¼ļĀłņĢäĒŗ┤ĒéżļéśņĢäņĀ£Ēśłņ”ØņØ┤ļØ╝ļŖö ņä£ļĪ£ ļŗżļźĖ ņ×äņāü ņ¢æņāüņØä ĒÖĢņØĖĒĢśņśĆļŗż. CAV3 ņ£ĀņĀäņ×ÉņØś ļ│æņøÉņä▒ ļ│ĆņØ┤ļź╝ Ļ░¢ļŖö ĒÖśņ×ÉņØś ļŗżņ¢æĒĢ£ ņ×äņāüĒæ£ĒśäĒśĢņŚÉ ļīĆĒĢ£ ņØĖņŗØņØĆ ĒÖśņ×ÉņØś ņ¦äļŗ©Ļ│╝ ņ£ĀņĀäņāüļŗ┤ņŚÉ ņżæņÜöĒĢśņŚ¼ ņØ┤ļź╝ ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.