서론
감각자극, 운동, 또는 특정 상황에서 자극을 주었을 때 일정한 시간 내에 나타나는 신경계의 전기적 반응을 유발전위(evoked potential)라고 한다[1]. 특히, 시각자극을 줄 때 시각계에서 유발된 반응을 시각유발전위(visual evoked potential, VEP)라고 한다[1]. 한 번의 자극에 의한 반응은 진폭이 너무 작아 자극과 관계없는 주변잡음(background noise)으로부터 구별하기 어렵기 때문에, 여러 번의 자극에 의한 반응을 평균화(averaging)하는 과정을 통해 유발전위를 구별해 내는 과정이 필요하다[1]. 또한 자극 종류, 자극 조건, 증폭기의 조건, 기록 조건 등의 비생리적인 요인과 환자의 신체 조건 등과 같은 생리적 요인에 따라 결과가 매우 상이하게 나타날 수 있다[1]. 따라서, 각 검사실마다 이에 대한 조건을 표준화한 상태에서 얻어진 결과로 분석하는 것이 필수적이다[1,2]. 본고에서는 시각유발전위의 검사 방법, 파형의 의미, 임상적용 및 분석 방법 등에 대해 전반적으로 기술하고자 한다.
본론
1. VEP의 기본 원리 및 종류[1-3]
VEP는 시각 자극에 의해 유발되는 전기생리적 전위이다. VEP는 실제 진폭이 매우 낮아 뇌파에 혼합되어 기록되어 그 파형을 구별해내기 어렵다. 따라서 주위 파형을 상쇄하고 작은 진폭의 유발전위를 명확하게 하는 평균화 과정이 필요하며, 임상에서 VEP가 응용되기 시작한 것은 컴퓨터 기술이 발달한 1970년대 중반부터이다.
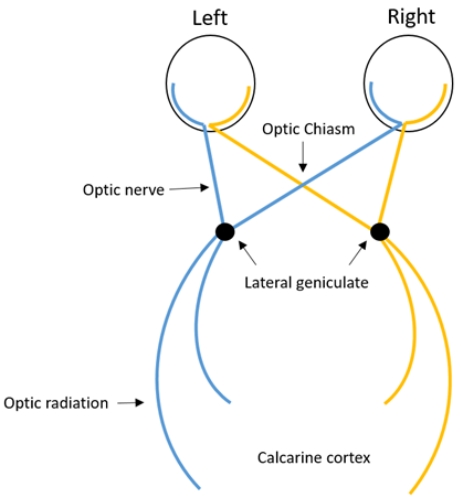
VEP 검사는 시각자극에 대해 망막에서 시신경, 시각교차(optic chiasm), 시각로(optic tract), 외측무릎체(lateral geniculate body), 시각로부챗살(optic radiation)을 거쳐 일차시각피질(primary visual cortex Brodmann’s area 17)에 도달하기까지의 경로를 검사할 수 있다. 이 경로 중 시신경은 시각 교차(optic chiasm)에서 일부는 반대쪽(contralateral side)으로 교차되며, 이에 따라 우측 시야(visual field)의 정보는 좌측 시각로(optic tract)로 좌측 시야의 정보는 우측 시각로로 전달된다(Fig. 1).
임상에서 활용되는 VEP들은 다음과 같이 시각자극의 종류나 방식 등에 따라 구분된다. 자극의 종류에 따라서 패턴화된 자극을 사용하는 경우를 패턴 시각유발전위(pattern VEP, PVEP), 패턴화되지 않은 자극인 섬광(flash)을 사용하는 경우를 섬광유발전위(flash VEP, FVEP)로 크게 구분할 수 있다. VEP의 개발 초기에는 시각자극을 위해 광자극(flash stimuli)이 사용되었는데, 광자극에 의해 유도되는 유발전위는 파형은 비교적 분명하게 기록되나 사람 간(inter-individual) 또는 같은 사람에 대해(intra-individual) 반복적인 검사를 시행하는 경우에 결과의 차이가 커서 임상적 유용성이 떨어졌다. 이후, 시각 중추 대뇌피질의 신경세포는 일반적 광자 극보다는 일정한 규격의 복잡한 시각자극에 더 잘 활성화 된다는 점에 기초하여 패턴자극을 이용한 형태(PVEP)를 주로 사용하게 되었다. PVEP는 밝은 모양과 어두운 모양의 배열에서 명암이 서로 바뀌는 형태로, 임상적으로 제일 많이 사용하는 것은 비교적 간단하고 신뢰도가 높은 서양장기판 패턴(checkerboard pattern)이며, 그 외 막대나 사인곡선격자(sinusoidal grating)자극이 이용되기도 한다. 사인곡선격자자극은 피험자가 굴절 이상(refractive error)이 있을 경우 서양장기판 패턴에 비해 영향을 적게 받는다. PVEP는 격자의 크기, 자극 범위(field)의 크기 및 자극 범위의 위치를 시감각 경로의 특정 영역을 선택적으로 검사하기 위해 조정할 수 있다. 화면을 주시해서 보지 못하거나, 집중을 하지 못하는 환자 등 특별한 경우에만 광자극의 변형인 고글 시각유발전위(goggle VEP)가 이용되며, 이외 대부분은 패턴역전 시각자극 형태(pattern reversal VEP, PRVEP)를 사용하고 있다.
그 외 자극의 빈도에 따라서도 구분되는데, 4회/sec 이하의 자극 빈도를 주는 경우 일시적 시각유발전위(transient VEP)가 형성되며, 10회/sec 이상의 빈도로 자극 시에는 반응이 합쳐져 자극의 빈도에 따른 진동(oscillation)이 관찰되며 이를 안정 상태 시각유발전위(steady-state VEP)라 한다. 현재 임상에서는 일반적으로는 일시적 시각유발전위 방식이 주로 사용되고 있는데, 안정 상태 시각유발전위는 적절하게 정량화할 수 있는 상업적 기계만 만들어진다면 임상적으로 상당히 광범위한 유용성이 있을 것으로 기대된다.
2. VEP 검사의 실제
1) 패턴역전 시각유발전위(PRVEP) [2,3]
패턴 자극 후 100 ms 근처에 양성 정점(peak)이 후두엽 부위에서 관찰된다. 이 때 관찰되는 전위들은 나타나는 순서와 극성에 따라 N1, P1, N2로 명명하거나, 정상적으로 관찰 되는 잠복기와 극성을 조합하여 N75, P100, N145로 명명한다. 동시에 전두엽 부위에서는 N100 파형이 관찰된다(Fig. 2). N145는 반응이 일정치 않아서 임상적으로 활용되지 않으며, P1 (P100) 파형 분석이 임상적으로 중요하다.
(1) 자극 방법[1-4]
TV 화면을 통해 패턴 변화 자극을 주는 방식이 일반적으로 이용되며, 축을 중심으로 회전하는 거울 또는 LED 등을 이용하여 패턴 자극을 주기도 한다. 자극 방법으로 장기판 패턴, 막대, 점, sinusoidal grating 등이 있으며, 일반적으로 서양장기판 패턴을 이용한 transient VEP를 측정한다.
자극 시 빈도는 시각자극 변화에 따른 파형의 간섭현상을 방지하기 위해 4회/sec 이하로 하며, 1-2회/sec로 자극을 주는 것이 일반적이다.
자극 강도는 대조도(contrast)와 조도(luminance)를 조정하여 조절한다. 대조도는 체크 간의 밝기 차이(depth of contrast)이다. 체크 간의 밝기 차이는 체크의 밝은 부분의 밝기 (Lmax)와 어두운 부분의 밝기(Lmin)를 사용하여 contrast=(Lmax-Lmin)/(Lmax+Lmin)으로 계산하며, 0.5 (최고와 최저 조도가 3배 차이) 이상을 유지하도록 체크의 밝기를 조절한다. 대조도가 너무 낮으면 VEP의 잠시가 지연되고 파형이 작아진다. 조도는 밝을수록 진폭이 커지고 잠시가 짧아지며, 검사실에 따라 조도 차이가 있을 수 있어 일정하게 유지하도록 한다.
체크의 크기 또는 시야각은 검사 결과에 영향을 미치는 중요한 인자이다. 시야각(visual angle [VA], β)은 한 개의 체크가 망막에 투사된 크기를 의미한다. Tan β=a/b에서 a는 체크 하나의 길이(mm)이고, b는 피검자와 자극 사이의 거리(mm)로, 도(degree [°]) 또는 분(minute[’]) 단위로 계산된다. 체크 크기가 작을수록 VA는 작아진다. 중심시야인 황반(fovea)은 VEP파의 가장 많은 부분을 담당하며, 작은 체크 크기(작은 VA)에 민감하여 10’에서 가장 큰 반응을 보인다. 망막 주변부는 이보다 큰 체크 크기에 잘 반응한다. 일반적으로는 작은 체크(12-16’)는 중심시야를 검사하기 위해, 큰 체크(40-50’)는 주변 시야를 자극하기 위하여 사용하며, 전체적으로 검사할 때는 중간 크기의 체크(24-32’)를 사용한다. 체크 크기가 작을수록 VEP 진폭이 커져 검사의 감도는 증가하나 피검자의 시력과 화면조명 변화에 민감하다. 시신경염이 의심되는 경우 작은 체크로 자극을 주면 양성률을 증가시킬 수 있다.
자극을 주는 시야의 영역에 따라 전시야(full-field), 반시야(half-field), 중심시야(central-field), 부분시야(partial-field) 등으로 나눌 수 있다. 전시야는 주시점으로부터 양쪽 시야가 동등하게 자극되는 경우를 말하며, 반시야는 주시점의 한쪽 시야만 자극되는 경우를 말한다. 반시야 VEP는 전시야 VEP보다 시각교차점과 시각로, 시각로부챗살의 병변을 더 민감하게 나타낼 수 있다. 중심시야는 주시점 근처, 즉 2-4°의 작은 영역을 말하며, 부분시야는 시야 중 일부분을 자극하는 것을 말한다. 상부 또는 하부의 망막을 구분하여 자극할 수 있는데 상부 망막자극 시에 잠시가 더 짧고, 파형이 앞쪽으로 분포한다. 반시야나 부분시야 검사 시에는 주시점을 자극영역에서 1° 크기가 되는 체크 넓이만큼 떨어지게 하여, 무의식적인 안구운동에 의해 의도하지 않았던 시야가 자극되는 것을 막도록 한다.
대개 편측 눈을 자극하여 검사하며, 만일 양측을 동시에 자극하면 파형이 더 커지나 잠시는 비슷하다. 만일 편측 검사에서 한쪽 눈에 이상이 있어도 양측 눈을 동시에 자극하면 정상 VEP 소견으로 나올 수 있다.
(2) 기록 방법[1-3,5]
시각자극 시 거의 두개부의 전체에서 VEP 파형이 기록되나 부위에 따라 전위가 서로 다르게 나타난다. 일반적으로 P1이 뒤통수점(inion)에서 가장 크게 기록되나 피검자에 따라서 두정부에 더욱 잘 기록될 수도 있다. 따라서 기록 전극은 후두부 중앙과 좌우(Oz, O1, O2), 두정부(Pz)에 부착하고 기준 전극은 전두부 중앙(FPz)에 부착한다. 이 4개의 채널을 통해 자극하는 동측 및 반대측의 파형을 함께 기록한다.
좌측(O1-FPz), 우측(O2-FPz), 중앙 후두엽(Oz-FPz) 및 두정엽(Pz-FPz)의 몽타주를 이용한다. P100의 진폭이 작거나, 관찰되지 않는 경우 P100이 일반적인 위치가 아닌 조금 더 위쪽이나 아래쪽에 위치할 수 있으므로 기준 전극의 위치를 귀볼(A1, A2)로 변경하여 기록 전극을 뒤통수점, 후두 중앙, 두정부, 전두부의 기록 전극으로 다시 한 번 검사하여 진폭이 가장 큰 부위에서 기록해 보는 것이 도움이 된다.
주파수 영역(bandpass)은 1-100 Hz로 하며, 분석시간은 250 msec 정도로 한다. 평균화 과정을 거치기 위해 전시야의 경우 100회, 반시야의 경우 200회 자극을 주어 검사한다. 재현성(replication)을 보이기 위해 2회 이상 시행하여 2회이상 시행한 P100의 잠시 차이가 2.5 ms 이내이고, peak-to-peak 진폭 차이가 15% 이내일 때 기록한다.
피검자가 굴절 이상이 있는 경우는 시력을 교정하고 검사를 시행하여야 하며, 검사 전 시력을 측정하여야 한다. 지속적으로 하나의 점을 주시해야 하므로 이로 인한 눈의 피로 때문에 검사 결과에 영향을 미칠 수 있으므로, 피로를 최소한 줄이기 위해 자극기와 피검자 사이의 거리가 적어도 70 cm 이상 유지되어야 한다. 검사자는 검사 동안 피검자가 주의를 유지하고 있는지 관찰하여, 피검자가 주의 집중을 유지하도록 한다. 또한 동공의 크기도 검사 결과에 영향을 미칠 수 있으므로, 검사 전 동공의 크기를 조절하는 안약의 사용은 금한다. 그 외 동공의 크기가 비대칭이거나 매우 작거나 크면 잠복기와 진폭, 대칭성(symmetry)에 영향을 미치므로 특히 백내장이나 유리체 혼탁(vitreous opacity)이 같이 동반되어 있는 경우에는 결과 분석 시 감안해야 할 부분이다. 피검자는 보통 상태의 밝기에서 검사를 받게 되며 환자의 턱이나 목을 편안한 상태로 검사하여 근수축에 의한 간섭 등을 줄이고, 검사 시 조용한 상태를 유지하여 청각유발전위 등에 의한 간섭을 피하도록 한다.
(3) PRVEP에 영향을 미치는 인자들[1,3]
연령에 따른 요인을 고려해야 한다. 소아는 검사에 집중을 잘하지 못하여 종종 파형 기록이 잘 안되기도 하지만, 정밀하게 살펴보면 신생아에서도 파형이 발생된다. 1세가 되면 큰 체크 크기(50-60’)에 대한 잠시가 성인과 동일한 검사치에 이르고, 5세가 되면 작은 체크 크기(12-15’)에 대해서도 성인과 같은 잠시를 나타낸다. 성인에서는 60세 이후 유의하게 잠시가 연장되며 40대 이후 10세 증가 시 2-5 msec 씩 증가하여, 이에 따른 정상치 보정이 필요하다. 나이에 따른 잠시 변화는 조도가 약하거나, 체크 크기가 작을수록 뚜렷해지나, 진폭은 나이에 따른 변화가 뚜렷하지 않다. 여성에서 잠시가 다소 짧으나 정상치에 있어서 차이는 크지 않다.
시력에 따라 영향을 받는데, 시력이 0.1 미만이면, VEP 진폭이 감소되고, 약 20 msec 정도 잠시가 연장되는데, 이러한 반응은 작은 크기, 낮은 대조도의 체크 패턴에서 현저하게 나타난다. 우성인 눈에서 잠시가 더 짧고, 진폭이 큰 경향을 보이나 정상치에 영향을 주는 정도는 아니다.
자극 빈도가 영향을 줄 수 있으며, 시각 자극 변화에 따른 파형의 간섭 현상을 방지하기 위해 4회/sec 이하로 하고, 대개 1-2회/sec의 자극 빈도로 장기판 패턴 변화 자극을 준다. 자극 강도의 영향으로 대조도 또는 조도가 너무 낮으면 VEP의 잠시가 지연되고 파형이 작아질 수 있다.
체크 크기에 따라 영향을 받는데, 작은 체크 크기(12-16’) 는 중심시야를 자극하고, 큰 체크 크기(40-50’)는 주변 시야를 자극하며, 일반적으로 중간 체크 크기(24-32’)를 사용한다. 중심시야가 VEP의 많은 부분을 담당하므로, 작은 체크일수록 진폭이 증가되는 경향을 보이나 잠시는 변화 없다.
(4) PRVEP 결과 분석[1,3,6]
VEP 검사를 분석하기 위해서는 먼저 VEP 검사가 제대로 잘 시행되었는지를 확인해야 한다. 제대로 얻어진 VEP 유발전위도 실제적인 파형인지를 평가하기 위해 두 개의 유발전위를 얻어 각각 파형의 일치성을 확인한다.
전시야 VEP에서는 P100 잠시의 지연이 임상적으로 가장 의미 있는 소견이며, 환자의 상태에 가장 영향을 적게 받는 값으로, 일단 VEP가 얻어지면 P1 (P100)의 잠시, 진폭 등을 측정한 후 이상 유무를 판정한다. 안구나 망막의 병이 없는 경우 잠시의 이상은 시각경로의 이상을 반영한다. 한쪽 눈의 잠시만 지연된 경우는 한쪽 시신경의 이상을 의미하며, 양쪽 모두 잠시가 지연된 경우는 진폭의 비율이나 나타나는 위치에 대해 더 자세히 분석하지 않는 한 시각교차 전의 문제인지 시각교차 후의 문제인지 감별은 어렵다.
P100 진폭이나 진폭의 비율은 정상값이 정해져 있지 않다. 일반적으로 정상적인 반응은 안구 간 진폭의 비율이 2:1-2.5:1 이내이다. 진폭의 이상은 P100이 관찰되지 않거나, 비정상적으로 진폭이 낮거나, 양쪽 눈의 진폭의 차이가 클 때로 정의할 수 있다. 안구의 질환이 없고, 환자가 주시점을 잘 집중한 경우, 진폭의 이상은 시각경로의 이상을 의미한다. 진폭은 안구나 망막의 병변을 발견해내는 데에 잠시보다 민감하다.
P100은 경우에 따라서 두 개의 peak (bifid peaks)로 관찰 되기도 하는데, 잠시나 진폭에 이상이 없으면 큰 의미가 없다. 이는 시야장애가 있거나 시각피질의 상부와 하부에서 형성되는 전위가 차이가 날 경우에 발생될 수 있으며, 다른 부위에서 발생한 잡음에 의한 것일 경우와 감별이 필요하다. 시야장애에 의한 경우라면 더 외측의 전극에서 기록된 파형을 참조하여 진짜 P100을 확인하도록 한다. 상부와 하부의 시각피질의 형성 전위가 차이가 날 경우는 하부시야를 자극하여 상부시각피질에서만 반응이 나타나도록 하여 정확한 P100을 구해본다. 검사 결과에 따라 예측되는 병변의 위치를 Table 1에 정리하였다.
반시야 VEP에서 나타나는 반응은 전시야 VEP와 다른 점이 있다. 우선 자극되는 시야와 동측의 후두부에서 N75, P100, N145가 더 잘 관찰되며, 자극되는 시야의 반대쪽 시야에서 P75, N105, P135가 관찰된다(Fig. 3). 이는 일차시각 피질 대부분이 후두엽의 안쪽면에 위치해 있어 이곳에서 형성된 전위는 자극한 시야와 반대쪽의 두피 즉, 자극된 일차시각피질의 두피에서보다는 자극된 시야의 동측 두피(자극된 일차시각피질의 반대쪽 두피)에서 더 잘 기록되기 때문인데 이를 모순 제시(paradoxical presentation) 현상이라고 한다. 이 때문에 반시야 자극 시 반대쪽에서 나오는 N105는 후두부보다는 측두부에서 잘 기록되므로 좌우 후두엽 전극의 바깥쪽으로 5 cm에 위치한 LT/RT 전극을 추가로 이용하기도 한다. 전시야 VEP와 마찬가지로 P100 잠시와 진폭은 가장 의미 있는 지표이다. 반시야 검사에서는 P100이 없는 경우에도 P75와 P135는 관찰될 수 있어 P75나 P135를 P100으로 오인할 수 있다. 따라서 반시야 VEP에서 정확하게 P100의 정확한 구별이 중요한데, 자극의 같은 쪽 후두부 전극에서 P100이 잘 구별되므로 이 점을 이용하도록 된다. 검사 분석 시 P100의 잠시와 진폭을 구해서, 같은 시야 자극 시 양쪽 눈의 잠시와 진폭의 차이를 비교하고, 같은 쪽눈에서 오른쪽과 왼쪽 시야 자극 시의 잠시, 진폭의 차이를 비교한다. 반시야 VEP의 이상에 따른 병변의 위치를 Table 2 에 나타내었다.
2) 섬광유발전위(FVEP) [1,3]
FVEP는 PRVEP에 비해 병변을 잘 반영하지 못하기 때문에 1) 심한 굴절 이상으로 체크를 구별 못하는 경우나 2) 너무 어리거나 협조가 되지 않아 주시점에 고정 못하는 경우에만 사용한다. 섬광 자극 후 250 ms 이내에 7개의 peak가나타나며, 각 peak의 잠시는 개인별 차이가 있고 또한 피검자의 각성 상태에 따라 변화가 심하다.
자극하는 방법으로 패턴화되지 않은 광선이 사용되는데 일반 뇌파 검사에서 사용하는 것과 유사하며, 임상에서는 LED가 부착된 고글이 주로 사용된다(goggle VEP). 자극 빈도는 1-2회/sec로 하며, 한쪽 눈씩 자극하는 것이 좋다.
하나의 중앙 후두부 전극만으로도 FVEP 유무를 충분히 확인할 수 있으나, 만약 전위가 형성되지 않으면 더 많은 채널을 사용한 몽타주가 필요하며, 따라서 PRVEP와 같은 몽타주가 사용된다.
FVEP는 개체 간의 변이가 크기 때문에, 반응이 나타나지 않을 경우에만 확실하게 이상이 있다고 할 수 있다. 진폭이나 잠시가 양쪽에서 의미 있게 차이가 난다면 낮은 진폭이나, 긴 잠시를 가지는 쪽의 문제라고 할 수 있다. 또한 영아나 협조가 되지 않는 환자에서 FVEP가 관찰된다고 하여도, 이것이 피검자가 시각정보를 자각하는 것을 증명한 것이라고 할 수는 없다. 반응이 관찰된다는 것은 시각 정보가 대뇌 후두엽까지 전달된다는 것을 의미하지만 중심시야나 주변시야 중 일부분만 정상이어도 정상 소견을 보일 수 있고 피질시각상실(cortical blindness)에서도 정상 소견을 보일 수 있어 피험자가 시각 정보를 지각하는 것과는 다른 문제이다.
결론
최근 정밀한 뇌영상 검사의 개발로 신경생리학적 검사의 임상 유용성이 다소 떨어지고 있는 것은 사실이나, 아직 뇌파, 유발전위, 근전도 등 임상신경생리 검사의 특정한 분야는 신경해부학적 진단 또는 뇌영상 검사에 의한 대체가 불가하다. 시각유발전위 검사는 시각회로의 신경생리적 기능을 평가할 수 있어 시각 기능의 연구에 있어 매우 중요한 도구이며, 최근 multifocal patterned VEP, multichannel VEP 등 새로운 기법들이 개발되어 기존 시각유발전위 검사의 제한점들이 개선되고 있다[4,6]. VEP 검사시 검사자와 피검자의 협조는 매우 중요하며, 최적의 상태에서 규격화된 검사 기법에 따라 VEP 검사를 시행하였을 때 일정한 검사 결과를 얻을 수 있으며 예민한 변화의 평가가 가능하므로 검사법에 대한 숙지와 판독법의 이해는 매우 중요하다.